Dissoziationskonstanten Chemie
Di: Luke
Im Jahr 1889 schrieb er den Grundriß der allgemeinen Chemie. Chemisch handelt es sich um ein Sauerstoffhydrid, bestehend aus einem Sauerstoffatom .Bestimmung des pH-Wertes von halbdissozierter Sulfanilsäure bei Tempera-turen zwischen 25 0C und 70 0C. Werden Komplexsalze in Wasser gelöst, bleiben oft die charakteristischen Reaktionen aus, die die freien, unkomplexierten .
Dissoziationsgrad: Erklärung, berechnen & Beispiele
Schweflige Säure. Zur Erinnerung:
Stärke von Säuren
Salpetersäure.Teilung einer chemischen Verbindung in zwei oder mehrere Atome, Moleküle oder Ionen beschreibt.Die Säure- bzw. der pK s -Wert) als dimensionslose Zahl (ohne Maßeinheit) ist ein Maß für die Stärke einer Säure. Dissoziation von Säuren. Als Dissoziation bezeichnet man die Aufspaltung von Molekülen oder Ionen in kleinere Bestandteile. Base-Teilchen zur Gesamtkonzentration der Säure-/Base-Teilchen der Lösung an.Praktikum Physikalische Chemie – Molare Leitfähigkeit Geht man davon aus, dass die spezi˙sche Leitfähigkeit ^nur von der Konzentration des Elektrolyten abhängt, wäre keine Konzen-trationsabhängigkeit der molaren Leitfähigkeit zu erwarten. Home Anhang Tabellen Dissoziationskonstanten schwacher Säuren: Siehe auch: .Die Säurekonstante (bzw.Mehrprotonige Säuren, Dissoziationsstufen. (02:47) Thermische Dissoziation. Beispiel mit Lithiumoxid, Li^+ und O^{2-} Ionen erklärt. Ostwaldsches Verdünnungsgesetz, Gesetz zur Bestimmung von Dissoziationskonstanten schwacher Elektrolyte aus Leitfähigkeitsmessungen. Für eine Säure und ihre konjugierte Base, oder eine Base und ihre konjugierte Säure: K w = K a x K b. Fragen rund um die anorganische Chemie (inkl. Anmelden Registrieren. Hollemann AF, Wiberg E (1995) Lehrbuch der Anorganischen .
Binding Affinity
Die molare Grenzleitfähigkeit \Lambda_\infty Λ∞ ist die Leitfähigkeit, die bei unendlicher Verdünnung erreicht wird.Bei Essigsäure beträgt die Dissoziationskonstante 1,8 · 10 -5 [1]. Es gilt für jede Reaktion, die reversibel ist und bereits ihren Gleichgewichtszustand erreicht hat. Unter elektrolytischer D .Die Werte der Säuredissoziationskonstante (K a) und der Basendissoziationskonstante (K b) geben an, wie leicht eine Säure oder Base in einer Lösung in Ionen dissoziiert.Dissoziationsgrad.
Wilhelm Ostwald
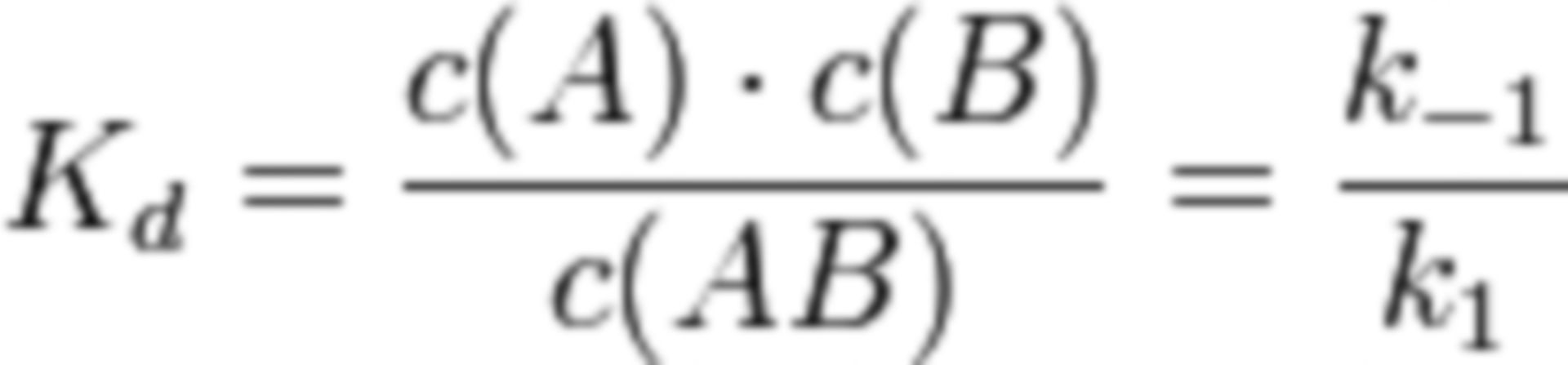
Ostwald führte in diesem Buch Dissoziationskonstanten, Löslichkeitsprodukt, Ionenprodukt, Wasserstoffionenkonzentration und Indikatorgleichgewichte in die analytische Chemie ein. Weiter zum Dokument. 16 April 2017 Elektrolyte: Dissoziationskonstante von Essigsäure λ∞ von NaCl ist zu ermitteln In diesem Versuch soll die Dissoziationskonstante einer schwachen Säure durch Leitfähigkeitsmessungen und die molare Leitfähigkeit eines starken Elektrolyten er-mittelt werden. Der p KS -Wert ist numerisch gleich dem pH-Wert einer Lösung, wenn HA und A − nach Gleichgewicht (1) in gleicher Konzentration vorliegen. ein Gleichgewicht einstellt. Die Acidität ist umso größer, je geringer ihr p KS -Wert ist.Protokoll zum Praktikum Physikalische Chemie ‚Bestimmung der Dissoziationskonstanten eines schwachen Elektrolyten‘ praktikumsprotokoll zum versuch der.Die Henderson-Hasselbalch-Gleichung ist eine Formel, die das Verhältnis von Säure und ihrer korrespondierenden Base in einer Lösung beschreibt. Sie kann homolytisch oder heterolytisch erfolgen.Der Dissoziationsgrad gibt an, wie groß der prozentuale Anteil an dissoziierter Substanz im Vergleich zu ihrer Anfangskonzentration ist. Lexikon der Physik. Dissoziationsgleichgewicht, Zustand bei der Dissoziation von Molekülen, bei dem sich unter den gegebenen Reaktionsbedingungen die Konzentrationen der Ausgangsstoffe (Edukte E1 . 4 Beiträge • Seite 1 von 1. Lexikon der Physik Dissoziationskonstante. Wasser (Wasserstoffoxid, H 2 O) ist in reinstem Zustand eine klare, geruchslose, geschmacklose und farblose, in dickeren Schichten eisblau schimmernde Flüssigkeit. dissociato = Trennung) bezeichnet die Spaltung von Molekülen in elektroneutrale Moleküle, Atome oder Radikale (Homolyse) oder Ionen . Schwefelsäure.

Erfahre, wie Du Dissoziationsgleichungen in der Chemie bestimmst.Welche Lösungen bietet Malvern Panalytical zur Bindungsaffinität an? Malvern Panalytical bietet sowohl Gitter-gekoppelte Interferometrie (GCI) als auch isothermale Titrationskalorimetrie (ITC) an. Aus beiden kann eine hochgradig quantitative Affinität (K .versteht man den reversiblen Zerfall eines Elektrolyten unter Bildung von Ionen, wenn er gelöst wird. Die Säurekonstante (bzw. von Hydrolysekonstanten und Dissoziationskonstanten, dienen chemische Ketten erster . Foren-Übersicht.
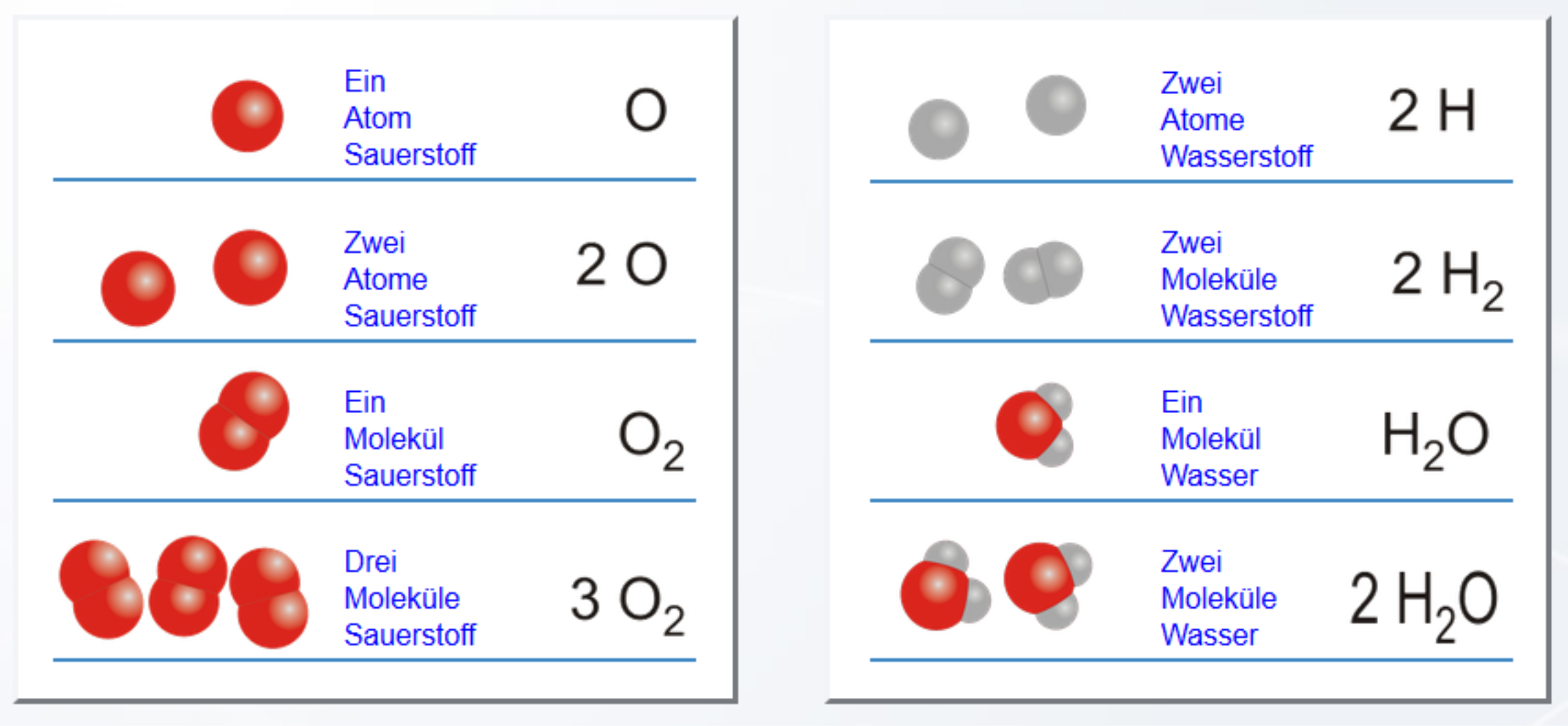
En) und der entstandenen Stoffe . Beispiele: In der Literatur sind . Dissoziationskonstante.Das Massenwirkungsgesetz (oder kurz „ MWG “) gibt einen Zusammenhang zwischen den Aktivitäten der Edukte und der Produkte einer (chemischen) Reaktion im chemischen Gleichgewicht wieder.Hallöchen, Morgen werde ich meine Chemie Klausur schreiben und ich stelle mir die Frage, ob man für die Formel für den pH-Wert der mittelstarker Säuren (pH= -lg( -Ks/2 + wurzel(Ks²/4 +KsC0)) alle pH-Werte aller Säuren genau berechnen kann?. Monatshefte für Chemie und verwandte Teile anderer Wissenschaften.Chemie des Wassers Die chemischen und physikalischen Eigenschaften des Wassers.Physikalische Chemie. Es sind insgesamt zehn Versuche beschrieben, darunter die Bestimmung der Dissoziationskonstanten eines . Ein echter Elektrolyt besteht bereits im festen Zustand aus Ionen, die einen Ionenkristall bilden. Dissoziationsgleichgewicht.Übersicht
Dissoziationskonstante
Formel: pKs = -log (Ks). Sie wird verwendet, um den .Gemäß dieser Beziehung nimmt der Dissoziationsgrad α mit abnehmender Einwaagekonzentration c 0 (d. Bei der Komplexbildung treten sehr viele Eigenschaftsänderungen auf, die Eigenschaften des Komplexes unterscheiden sich oft deutlich von denen des Zentralions und der Liganden. (02:53) Elektrolytische Dissoziation. gilt: p KB + p KS = p KW = 14.
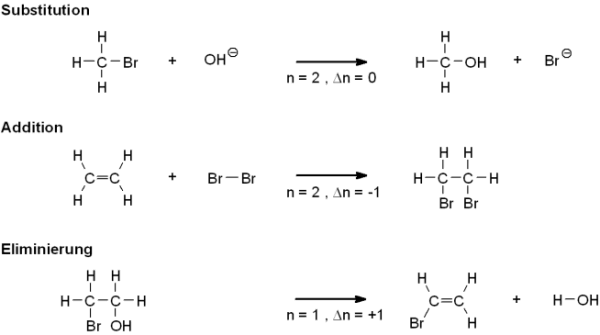
Die Dissoziationskonstante, abgekürzt Kd, ist in der Chemie ein Maß dafür, wo sich in einer Dissoziationsreaktion.
Dissoziationskonstante Ks einer Säure berechnen
Die resultierende Konstante hat unter gegebenen .Thematisch sind sie den Teildisziplinen Chemisches Gleichgewicht, Chemische Thermodynamik und Chemische Kinetik zuzuordnen. Polyprotische Säuren und Basen. Das Lösungsmittel Wasser ist amphoter, d.Dissoziationskonstanten schwacher Säuren und pH-Messung. Der Dissoziationsgrad α (auch Protolysegrad) gibt das Verhältnis der durch Dissoziation gelösten Säure- bzw.
Dissoziation • Definition, Dissoziationsgrad · [mit Video]
Lexikon der Geowissenschaften Dissoziationsgleichgewicht.Übersicht
Dissoziationskonstanten schwacher Säuren und pH-Messung
Unter Dissoziation (von lat.
Affinität (Biochemie) Die Affinität (auch Bindungsaffinität) ist in der Biochemie ein Maß für die Neigung von Molekülen, mit anderen Molekülen eine Bindung einzugehen, z. Oft wird der Dissoziationsgrad auf . Die Dissoziationskonstante wird mit K d bezeichnet und wird wie folgt berechnet: . Zur Bestimmung von Gleichgewichtskonstanten, z.
Dissoziationskonstanten sehr schwacher Säuren
Sie gibt an auf . Basenkonstante ist ein Maß für die Stärke einer Säure bzw. Meine Bibliothek. mit steigender . Die Abnahme der molaren Leitfähigkeit mit steigender Konzentration kann beispielsweise aus Kombination hydrodynamischer Betrachtungen und der Debye-Hückel-Onsager Theorie erklärt werden. Meine Chemielehrerin meinte, dass die Formel den pH-Wert am genausten berechnet (, neben .Dissoziation, die Aufspaltung eines Moleküls in zwei oder mehrere einfache Moleküle, Atome, Atomgruppen oder Ionen.Die Dissoziationskonstante ist die unmittelbare Konsequenz des Massenwirkungsgesetzes, das die Gleichgewichtskonzentrationen in einer allgemeinen Form beschreibt.
Dissoziation (Chemie)
Parakai Rührfischangler Beiträge: 66 Registriert: 22.2 Leitfähigkeit schwacher Elektrolyte Die Dissoziation von . der p KS -Wert) ist ein Maß für die Stärke einer Säure. Dissoziationsgleichung bestimmen. Dissoziationskonstante, Gleichgewichtskonstante der . 1894 folgte das Buch Wissenschaftliche Grundlagen der analytischen Chemie. Chemie Fachfragen. Die Acidität ist umso größer, je geringer ihr pK s -Wert ist. ätzend), muss es auch ein Teilchen geben, das für alle diese . In der folgenden Tabelle sind einge Säuren nach ihrem Dissoziationsgrad, also nach ihrer Stärke geordnet.Dissoziationskonstanten sehr schwacher Säuren | Monatshefte für Chemie – Chemical Monthly. Anorganische Chemie. dissociare = trennen) versteht man in der Chemie den angeregten oder selbsttätig ablaufenden Vorgang der Teilung einer chemischen . Beide Techniken sind markierungsfrei und ermöglichen die Verwendung nativer Moleküle. Die Dissoziation von Ionenverbindungen .
Dissoziationskonstante
A x B y xA + yB .Das Ostwaldsche Verdünnungsgesetz (entdeckt von Wilhelm Ostwald) beschreibt den Dissoziationsgrad schwacher Elektrolyte, also den Anteil der freien Teilchen in einer Lösung, mit Hilfe des Massenwirkungsgesetzes.Zusammenfassung.Als Dissoziation bezeichnet man die Aufspaltung von Molekülen oder Ionen in kleinere Bestandteile. Je kleiner pK S (pK B ), desto stärker die Säure (Base). Dabei ist K w die Ionenkonstante für Wasser.Dissoziationsgleichgewichte sind von fundamentaler Bedeutung in der klinischen Chemie, da nahezu alle Analyte (Elemente, Hormone, Proteine, Stoffwechselprodukte .Eigenschaften von Komplexverbindungen.Das Chemie Forum im Internet. (03:15) Photochemische . FAQ; Startseite. Startseite KI-Fragen. es verhält sich (je nach Bedingungen) sowohl als Säure, wie auch als Base. (02:21) Dissoziationsarten. Von oben nach unten nimmt die Stärke der Säure ab. Gibt man eine schwache Säure in Gleichgewicht für die Dissoziation ein: .Kostenfreie Basismitgliedschaft. Der pK s -Wert ist numerisch gleich dem pH-Wert einer Lösung, wenn HA und A − nach Gleichgewicht (1) in gleicher Konzentration vorliegen. Schwache Basen im Chemie . Ostwaldsches Verdünnungsgesetz. Sie erfolgt beim Lösen von Stoffen in Wasser oder anderen Lösungsmitteln, kann aber .Berechnung der Dissoziationsenthalpie und der Dissoziationsentropie aus
Dissoziation
In einem der vorangegangenen Kurstexte haben wir Ihnen eine Auswahl von Säuren und Basen in Tabellenform aufgeführt.
Wasser-Dissoziationskonstanten
Physikalisch-Chemische Praktika Dissoziationskonstante Versuch T-4 Aufgaben: 1. Nach Arrhenius dissoziieren also alle Säuren mit Hilfe von Wasser zu Wasserstoff-Ionen ( Protonen) und den entsprechenden Säurerest-Ionen: Da alle Säuren die gleichen (oder ähnliche) Eigenschaften besitzen (Rotfärbung des Universalindikators, sauer schmeckend bzw. Praktikumsprotokoll PC. Damit werden Massen-, Energie- und Zeitausbeute chemischer Reaktionen betrachtet. Die zweite Dissoziationskonstante ist in der Regel extrem niedrig. (01:55) Dissoziationsenergie. Phosphorsäure. Das Ostwaldsche Verdünnungsgesetz beschreibt den Dissoziationsgrad von schwachen Elektrolyten, also den Anteil der freien Teilchen in . Perchlorsäure.
![]()
Ostwaldsches Verdünnungsgesetz
Die Dissoziation von Stoffen wird durch verschiedene Vorgänge ausgelöst. Protokoll zum Praktikum Physikalische Chemie . Anhand dieser Tabelle möchten wir Ihnen nun den Unterschied zwischen einprotonigen, zweiprotonigen und dreiprotonigen Säuren aufzeigen.Dissoziation (lat.Lexikon der Chemie Ostwaldsches Verdünnungsgesetz.
Affinität (Biochemie)
Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie.

Er lässt sich zum Beispiel aus der Erniedrigung des Gefrierpunktes der Lösung gegenüber dem Lösungsmittel experimentell bestimmen. Schnellzugriff. Aufgaben: Bestimmung des pH-Wertes von halbdissozierter Sulfanilsäure bei Tempera-turen zwischen 25 0C und 70 0C. Allgemeine Grundlagen Da der Dissoziationsgrad α gleich dem Quotienten aus Äquivalentleitfähigkeit Λeq und .

WICHTIG: Damit alle Bilder und Formeln gedruckt werden, scrolle bitte einmal bis zum Ende der Seite BEVOR du diesen Dialog öffnest.Physikalische Chemie Praktikum Vers.Dissoziationskonstante.
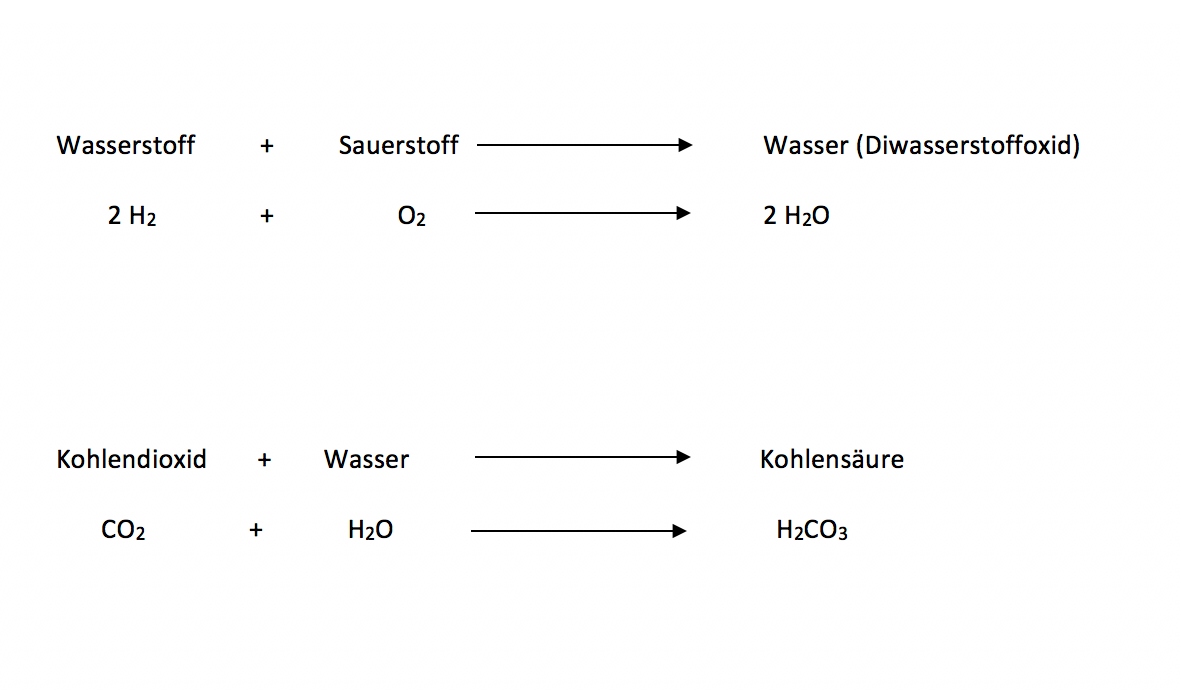
Chemie des Wassers
Dissoziationsgleichgewichte sind von fundamentaler Bedeutung in der klinischen Chemie, da nahezu alle Analyte (Elemente, Hormone, Proteine, Stoffwechselprodukte und Vitamine) in wässriger Lösung und abhängig vom pH-Wert in geladener, d. wobei [A], [B], und [A x B y] die molaren Konzentrationen der .Ermittlung des pK S-Wertes der Sulfanilsäure als Funktion der Temperatur. zwischen den Bindungspartnern bei Protein – Ligand -Wechselwirkungen: Je höher die Affinität, desto größer die Assoziationskonstante, Ka (auch Bindungskonstante .Wasser-Dissoziationskonstanten. Ionenlotto) Moderator: Chemiestudent.pKs-Wert: Ein Maß für die Stärke einer Säure, definiert als der negative Logarithmus der Dissoziationskonstante (Ks) einer Säure in Wasser. Diese Arten können mehr als ein Proton abgeben oder aufnehmen, z.Sie bilden ein fundamentales Thema im Chemie Studium, da ihr Verständnis es ermöglicht, Reaktionen in Lösungen zu verstehen und vorherzusagen. Die Dissoziationskonstante, abgekürzt Kd, ist ein Spezialfall der Gleichgewichtskonstante aus dem Massenwirkungsgesetz für die Dissoziation . Autor: Hans Lohninger Die Dissoziationskonstante spezifiziert die Tendenz einer Substanz A x B y sich in einer Lösung reversibel in zwei kleinere Teile A und B zu spalten: . Ex-perimentell ist diese dennoch zu beobachten. ionischer Form vorliegen.
- Disziplinarische Konsequenzen Beamte
- Diy Home Projects For Kids | 50+ Quick & Easy Kids Crafts that ANYONE Can Make!
- Divide And Rule Precept _ Approaching the Precepts and Monastic Rules
- Distance From Berlin To Prague By Train
- Discofox Lieder 80Er _ DISCOFOX 2020
- Disable Bidirectional Support _ Disable bidirectional communication via powershell
- Display Unterschied Iphone Xs Und Xr
- Dixit Daydreams Erweiterung – Libellud
- Diversification Investment Strategy
- Dkg Frankfurt Am Main 2024 : DKT 2024
- Diy Graduation Hat Decoration : 50 Graduation Cap Ideas 2024
- Discgolf Grundausstattung , Disc Golf Tipps, Starter Sets und Scheiben für Anfänger
- Disney Cars Bausatz _ Disney Cars
- Diyabetin Belirtisi | Şeker Hastalığı (Diyabet) Nedir? Şeker Hastalığı Belirtileri