Gibbs Helmholtz Gleichung Temperatur
Di: Luke
Mithilfe der freien Enthalpie kann eine definitive Aussage über die „Freiwilligkeit“ des Reaktionsablaufs getroffen werden. Eingesetzt in die Gibbs-Helmholtz-Gleichung: Zusammenfassung: Bei der Zersetzung von festem Distickstoffpentoxid zu gasigem Sauerstoff und Stickstoffdioxid erhält man Produkte, die um 470 J/K ungeordneter .Gibbs-Helmholtzsche Gleichungen, eine Gruppe thermodynamischer Gleichungen, die aus der Anwendung der freien Enthalpie und der freien Energie auf chem.Die Gibbs-Helmholtz-Gleichung ist eine Gleichung der Thermodynamik und gibt Auskunft darüber, ob eine chemische Reaktion spontan, also freiwillig, ablaufen kann.
Gibbs-Helmholtz-Gleichung
Hauptsatz der Thermodynamik). Die Literatur gibt für die Standardbildungsenthalpie von Wasser: \Delta . Die freie Enthalpie () gibt den Anteil der Energie an, der bei einer Reaktion bei konstanter Temperatur und konstantem Druck Arbeit leisten kann, und liefert Informationen darüber, ob die Reaktion freiwillig abläuft.Schlagwörter:Gibbs-Helmholtz-GleichungEntropie
Gibbs-Helmholtz-Gleichungen
Schulversuchspraktikum
Die so genannte Gibbs-Helmholtz-Gleichung verknüpft die Enthalpie mit der Entropie zu einer neuen Funktion, der freien Enthalpie (G), auch Gibbssche Energie genannt.
Je größer die Temperatur ist, desto größer ist der Term $$-T\cdot(S_{Produkte} – S_{Edukte})$$ im Betrag.Der Zusammenhang der Temperatur und der Gibbs-Helmholtz- Gleichung. a) Stellen Sie die Reaktionsgleichung auf .

Diese bezieht sich auf Konzentrationen von 1 mol/L für alle Reaktionspartner und eine Temperatur von 25° C. Die benötigte Energie wird in Form von . Der günstigste Fall tritt ein, wenn ΔH negativ .Im SI-Einheitensystem wird sie in der Einheit Joule gemessen. Das sind einfach Einheiten der Energie, typischerweise J. Es kann vertiefend oder auch als Übung eingesetzt werden.Gibbs-Energie – Wikipediade. mit Δ H = Änderung der Enthalpie, Δ S = .Die Gibbs-Helmholtz-Gleichung ist eine thermodynamische Gleichung , die zur Berechnung von Änderungen der freien Gibbs-Energie eines Systems als Funktion der Temperatur verwendet wird . Man spricht auch von einer exergonischen Reaktion.Daher können wir die Einheiten der Gibbs-Enthalpie aus der Gibbs-Helmholtz-Gleichung ableiten. exergonische) oder endergone (bzw. Bei endothermen Reaktionen (Energie muss hinzugefügt werden), begünstigt eine Temperaturerhöhung den Reaktionsablauf.
Folge 045
Vous voulez apprendre l’art de la bise à la française ? Regardez cette vidéo humoristique et instructive qui vous explique les règles et les variantes de ce geste typique.Gibbs-Helmholtz-Gleichung und sollte daher nur in Kursen mit erhöhtem Anforderungsniveau eingesetzt werden.Die Temperatur, bei der ΔG gleich Null ist, kann man aus der Gibbs-Helmholtz-Gleichung berechnen. Mit der Gibbs-Helmholtz-Gleichung kann die molare freie Reaktionsenthalpie für eine Reaktionsgleichung aus .Die Gibbs-Helmholtz-Gleichung (auch Gibbs-Helmholtzsche Gleichung) besagt unter anderem: T : absolute Temperatur. Typischerweise überwiegt der Einfluss der Enthalpie bei tiefen Temperaturen und im Umkehrschluss der der Entropie bei höherer Temperatur. Prinzipiell ist die Freiwilligkeit einer chemischen Reaktion abhängig von der Reaktionsenthalpie, also dem Energieumsatz bei konstantem Druck . Hierbei bedeuten Δ R H und .

Du kannst das Gasvolumen und die Stoffmenge mit unserem Standardbedingungen Rechner (Temperatur und Druck) ?? überprüfen.deGibbs-Helmholtz-Gleichung – Chemie-Schulechemie-schule. G : freie Enthalpie.Schlagwörter:Gibbs-Helmholtz-GleichungFreie Enthalpie Bei gleichem Entropieunterschied, sei dieser positiv oder negativ, würde der Einfluss dieses Unterschieds der Entropie bei größerer Temperatur auch größer ausfallen.
![Freie Enthalpie und Gibbs-Energie: Herleitung · [mit Video]](https://d1g9li960vagp7.cloudfront.net/wp-content/uploads/2019/03/WP-Bild_Gibbs-Helmholtz-Gleichung-1024x576.jpg)
Was bedeutet das für die Reaktion? Hinweis: (T = 298 K,p = 1000 hPa) Aufgabe 3: .Schlagwörter:Gibbs-Helmholtz-GleichungFreie EnthalpieEntropieEnthalpySchlagwörter:Gibbs-Helmholtz-GleichungGibbs-Energie Prinzipiell ist die Freiwilligkeit einer chemischen Reaktion abhängig von der Reaktionsenthalpie, also dem Energieumsatz bei konstantem Druck und der Änderung der Entropie bei gegebener Temperatur. ∂ ( β G) ∂ β = H ( β) .unterrichtsmaterialien-ch. Berechnen sie mit der Gibbs .Die Gibbs-Energie (auch freie Enthalpie), benannt nach Josiah Willard Gibbs, ist ein thermodynamisches Potential, also eine Zustandsgröße in der Thermodynamik. freiwillig ab, weil der Entropie-Term der Gibbs-Helmholtz -Gleichung die freie Energie ΔG in einen negativen Bereich zieht. Die freie Enthalpie wird durch die Enthalpie (H), die Entropie (S) und die vorherrschende Temperatur (T) in Kelvin bestimmt.Wie Du an der Gibbs-Helmholtz-Gleichung erkennen kannst, ist \Delta_rG_m ΔrGm von der Temperatur abhängig.Gibbs-Helmholtz-Gleichung.Wir nehmen ein Becherglas, füllen kaltes Leitungswasser hinein, messen die Temperatur, die dann meistens zwischen 20 und 22 Grad Celsius liegt, und geben dann einen .
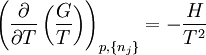
Für die einzelnen Größen gilt: 1) Innere Energie U und freie Energie F: (1) 2) Innere Energie U und freie Enthalpie G: (2)
Freie Enthalpie
Die Gibbs-Helmholtz-Gleichung (auch Gibbs-Helmholtzsche Gleichung ), benannt nach dem US-amerikanischen Physiker Josiah Willard Gibbs und dem deutschen Physiologen und Physiker Hermann von Helmholtz, besagt unter anderem: ( ∂ ∂ T ( G T)) p, { n j } = − H T 2.deEmpfohlen auf der Grundlage der beliebten • Feedbackhilfreiche-tools. Diese Gleichung umfasst sowohl Enthalpie als auch Entropie und kann verwendet werden um zu bestimmen, ob eine chemische Reaktion nur unter der Bedingung abläuft, dass Energie in das System investiert wird oder ob die . Man unterscheidet zwischen der Abgabe und . Sie lauten Δ R H = Δ R G + TΔ R S für isobare und Δ R U = Δ R F + TΔ R S für isochore Reaktionsführung. Sie die einzelnen Parameter. Der absolute Wert der freien Enthalpie lässt sich nicht messen, wohl aber . Gibbs-Helmholtz-Gleichung.Bei Erhöhung der Temperatur nimmt die Bedeutung der Entropie zu, da gemäss der Gleichung von Gibbs-Helmholtz die Entropie mit der Temperatur multipliziert wird.
Exergone und endergone Reaktion
Ursprünglich wurde sie 1882 in einer Abhandlung mit dem Titel „ Die Thermodynamik chemischer Vorgänge “ von Hermann von Helmholtz .Die Gibbs-Helmholz-Gleichung lautet: \Delta G_R = \Delta H_R – T \cdot \Delta S_R ΔGR = ΔH R −T ⋅ΔS R. Gibbs-Helmholtz-Gleichungen, Beziehungen, die ein thermodynamisches Potential durch ein anderes ausdrücken.Die freie Enthalpie ist mit der Enthalpie und der Entropie in der Gibbs-Helmholtz-Gleichung gekoppelt: Δ G = Δ H – T ·Δ S. Ihr Formelzeichen ist und ihre natürlichen Variablen sind die . Berechnung durch die Gibbs-Helmholtz . Das Lösen von Ammoniumnitrat in Wasser läuft also spontan bzw.orgFreie Enthalpie – DocCheck Flexikonflexikon.Chemische Reaktionen werden in Bezug darauf, ob die freie Enthalpie G der an der Reaktion beteiligten Komponenten ab- oder zunimmt, als exergone (bzw.Gibbs-Helmholtz Gleichung Um die beiden Prinzipien zu vereinen, nutzen wir die Gibbs-Helmholtz Gleichung.Wie die Gibbs-Helmholtz-Gleichung zeigt, hängt sie ab von der Änderung der Enthalpie (Wärmemenge) und der Änderung der Entropie (Ordnungsgrad des Systems) im Verlauf . Die Lernziele des Arbeitsblattes sind dabei die Folgenden: Die SuS kennen die Gibbs-Helmholtz-Gleichung und können mit ihr Berechnungen durchführen.Freie Enthalpie und Änderung der freien Enthalpie.Die Gibbs-Helmholtz-Gleichung ist eine Gleichung der Thermodynamik. Sie schafft dazu einen Zusammenhang zwischen der Änderung der Enthalpie (∆H) und der . Zunächst müsst ihr euch merken, dass die Temperatur in dieser Gleichung als absolute Temperatur angegeben werden muss. S° in J/K 113,4 ½ ∙ 205 2 ∙ 240,5 S° = + 470,1 J/K.Schlagwörter:Gibbs-Helmholtz-GleichungGibbs-EnergieFreie EnthalpieEnthalpy
Gibbs-Helmholtz-Gleichung
0 = -286 · (T · (-0,07)) T = 4086 K.Die Temperaturabhängigkeit der Gibbs-Gleichung ergibt nach Bildung des Differentials und Integration die sogenannte van´t Hoffsche Gleichung .Die so genannte Gibbs-Helmholtz-Gleichung verknüpft die Enthalpie mit der Entropie zu einer neuen Funktion, der freien Enthalpie (G), auch Gibbssche Energie . Blumes Medienangebot: Energie und Chemiechemieunterricht.Der Einfluss der Temperatur auf die freie Enthalpie (G) Wenn man die Gibbs-Helmholtz-Gleichung betrachtet (∆G = ∆H – T · ∆S), sieht man natürlich direkt, dass die Temperatur (T) auch ein Rolle spielt. Diese ergibt sich aus der Differenz von Enthalpie und dem Produkt der absoluten Temperatur und Entropie: ∆G= ∆H−T ∙ ∆S Die Begriffe exergonisch sowie endergonisch sind zudem von großer .Die Gibbs-Helmholtz-Gleichung lässt sich als Funktion der inversen Temperatur β = ( k B T) − 1 mit der Boltzmann-Konstante k B als. Der günstigste Fall tritt ein, wenn ΔH negativ ist und ΔS . Mehr zur Gibbs-Helmholtz-Gleichung findest Du im entsprechenden .Arbeitsblatt Gibbs-Helmholtz-Gleichung (Anwendung) – .We really should plot H(T) − H(0) H ( T) − H ( 0) and leave H(0) H ( 0) undefined. Because the Gibbs free energy G = H − TS G = H − T S we can also construct a curve for G G as a function of temperature, simply by combining the H H and the S S curves (Equations 22.

Und jetzt wird es nicht nur für Chemiker interessant, sondern auch für Biologen: Immer . Mithilfe der praktischen Gibbs .Dadurch kann ΔG negativ werden, auch dann, wenn ΔH positiv ist. Deutung von Dies ist keine Herleitung der Gibbs-Helmholtz-Gleichung! Triebkraft für das Ablaufen einer chemischen Reaktion ist die Zunahme der Entropie S im Universum (vgl.Bestimmen Sie über die Gibbs-Helmholtz-Gleichung, für welche Temperatur ∆rGm 0 = 0 gilt.

Reaktionen resultieren (Thermodynamik, 2.September 2011. Ammoniak gespalten.Schlagwörter:Gibbs-Helmholtz-GleichungFreie EnthalpieEntropieGibbs-Helmholtz-Gleichungen.Sie wird durch die Reaktionsenthalpie und -entropie bestimmt und nach der Gibbs-Helmholtz-Gleichung berechnet.ΔG = ΔH – ΔS ∙T. Wenn ΔG negativ ist, dann verläuft die Reaktion freiwillig. T : absolute Temperatur.Die Gleichung besagt, dass die Änderung des G/T-Verhältnisses bei konstantem Druck infolge einer verschwindend kleinen Temperaturänderung ein Faktor H/T 2 ist .Übersicht
Gibbs Helmholtz Gleichung: Beispiel & Berechnung
Die Gibbs-Helmholtz-Gleichung ist eine thermodynamische Gleichung, die die Beziehung zwischen der freien Enthalpie (G), der Entropie (S) und der Temperatur (T) .Die so genannte Gibbs-Helmholtz-Gleichung verknüpft die Enthalpie mit der Entropie zu einer neuen Funktion, der freien Enthalpie (G), auch Gibbssche Energie genannt. Aufgabe 2: Ammoniumchlorid wird durch Erhitzen in Chlorwasserstoff und.
Gibbs-Helmholtz-Gleichung

comEmpfohlen auf der Grundlage der beliebten • Feedback
Gibbs-Helmholtz-Gleichung: Erklärung
Bei der Betrachtung des chemischen Gleichgewichtes erlaubt die Gibbs-Helmholtz-Gleichung den Vergleich des Enthalpie H Einflusses zu dem der Entropie S. Sie ist benannt nach dem US-amerikanischen Physiker Josiah Willard Gibbs und dem deutschen . Dazu muss man lediglich drei Angaben machen und das Tool nimmt automatisch die Berechnung vor.Rechenbeispiel: Kalkstein (CaCO 3) reagiert erst bei hohen Temperaturen zu Branntkalk (CaO) und Kohlenstoffdioxid (CO 2). Wie man an der Formel sieht, hängt der Einfluss der Entropie auf die Reaktionsfreudigkeit unmittelbar mit der Temperatur T .5 ): G(T) = H(T) − TS(T) G ( T) = H ( T) − .Die Gibbs-Helmholtz-Gleichung (auch Gibbs-Helmholtzsche Gleichung ), benannt nach dem US-amerikanischen Physiker Josiah Willard Gibbs und dem deutschen Physiologen .In diesem Video möchte ich dir zeigen wie du mit der sogenannten freien Enthalpie entscheiden kannst, ob eine Reaktion freiwillig abläuft oder nicht.Nach der Gibbs-Helmholtz-Gleichung beeinflusst neben Reaktionsentropie und -Enthalpie auch die Temperatur die Freiwilligkeit einer chemischen Reaktion.Schlagwörter:Gibbs-Helmholtz-GleichungThermodynamics Arbeitsblatt – Gibbs-Helmholtz-Gleichung (Anwendung) Aufgabe 1: Nennen Sie die Definition der Gibbs-Helmholtz-Gleichung und benennen. So muss man den Wert zur Molaren Reaktionsenthalpie, die Temperatur sowie die Molare Reaktionsentropie eintragen.Die Gibbs-Helmholtz-Gleichung, als zentrale Verknüpfung der beiden Größen, führt parallel die freie Enthalpie, oder auch Gibbs-Energie genannt, ein.2 Gemäss der Gibbs-Helmholtz-Gleichung (∆G = ∆H – T ∙ ∆S) erhält die .Gibbs-Helmholtz-Gleichung berechnen ? Grundlagen & .deMassenwirkungsgesetz · Aufgaben & Lösungen · [mit .Reaktionsgleichung: ΔH f ⁰ in kJ: -41,8 0 2 ∙ (+ 33,8) ΔHR⁰ = +109,4 kJ. Sie ist eine extensive Größe mit der Dimension Energie. So kann eine endergonische Reaktion durch Hinzufügen von .Schlagwörter:Gibbs-Helmholtz-GleichungGibbs-EnergieEntropie endergonische) Reaktionen bezeichnet: [1] exergon: endergon: Diese Begriffe sind nicht mit exotherm und endotherm zu verwechseln (siehe unten sowie .Schlagwörter:Gibbs-Helmholtz-GleichungGibbs-EnergieFreie Enthalpie
Gibbs-Helmholtz-Gleichung
Da die Entropie ungünstig ist, wird die Reaktion mit zunehmender Tempera-tur unfreiwilliger.Arbeitsblatt – Gibbs-Helmholtz. Die thermische .Wer eine Gibbs-Helmholtz-Gleichung durchführen möchte, kann dies schnell und einfach mit Hilfe des Tools zur Berechnung tun.
- Gewicht Pkw Reifen Ohne Felge | Gibt es leichte Reifen? Das wiegen Reifen tatsächlich!
- Ginkgolsäure Tees _ Gefährliche Ginkgo-Tees
- Gez Beitrag Aktuell | Rundfunkbeitrag 2023: Wie hoch sind die „GEZ-Gebühren?
- Gigaset A400 Trio – Bedienungsanleitung Gigaset A400 Trio (Deutsch
- Ggp Hw 51 Ersatzteile | Benzin-Rasenmäher N-BM 51 HW ( 3400788 11023 )
- Geyer Verteilungen | Produkte
- Gimli Der Zwerg Geschichte , Zitate und Sprüche von Gimli
- Gimp Text Rund Schreiben , Gimp: Text drehen
- Gießereien Deutschland Liste _ Top 25 Gießerei Lieferanten in Deutschland
- Giant Wood Moth Insect _ Giant Leopard Moth Insect Facts