Richtlinie Gewinnung Blutbestandteile
Di: Luke
Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie): aufgestellt von der Bundesärztekammer im Einvernehmen mit dem Paul-Ehrlich-Institut : Amazon.Die Gesamtnovelle 2023 ersetzt die Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie), Gesamtnovelle 2017, mit Erratum/Anpassungen 2019 und umschriebener Fortschreibung 2021.
Richtlinie Blutprodukte Gewinnung von Blut und Herstellung sowie Anwendung von Blutprodukten in der Zahnheilkunde Bundeszahnärztekammer, November 2023 Aufgestellt gemäß §§ 12a und 18 Transfusionsgesetz von der Bundeszahnärztekammer im Einvernehmen mit dem Paul-Ehrlich-Institut in der vom .
Richtlinie
Januar 2003 zur Festlegung von Qualitäts- und Sicherheitsstandards für die Gewinnung, Testung, Verarbeitung, Lagerung und Verteilung von menschlichem Blut und Blutbestandteilen und zur Änderung der Richtlinie 2001/83/EG. Februar 2017 auf Empfehlung des Wissenschaftlichen Beirats beschlossen, die Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie) gemäß §§ 12 und 18 des Transfusionsgesetzes (TFG) vom .Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie) Aufgestellt gemäß §§ 12a und 18 .Richtlinie setzen auch die europarechtlichen Vorgaben aus der Richtlinie 2002/98/EG. Richtlinie 2002/98/EG des Europäischen Parlaments und des Rates vom 27.Richtlinien – Novellierung 2005.3 Themen der Richtlinien Diesen Aufgaben entsprechend befassen sich die Richtlinien mit • allgemeinen Grundsätzen der Hämotherapie, Fragen ihrer Organisation, der not wendigen Qualifikation der Ärzte, der Zuständigkeit sowie haftungsrechtlichen Fragen (Kap.Die Richtlinie 2002/98/EG legt Qualitäts- und Sicher-heitsstandards für die Gewinnung und Testung von menschlichem Blut und Blutbestandteilen unabhängig von deren .

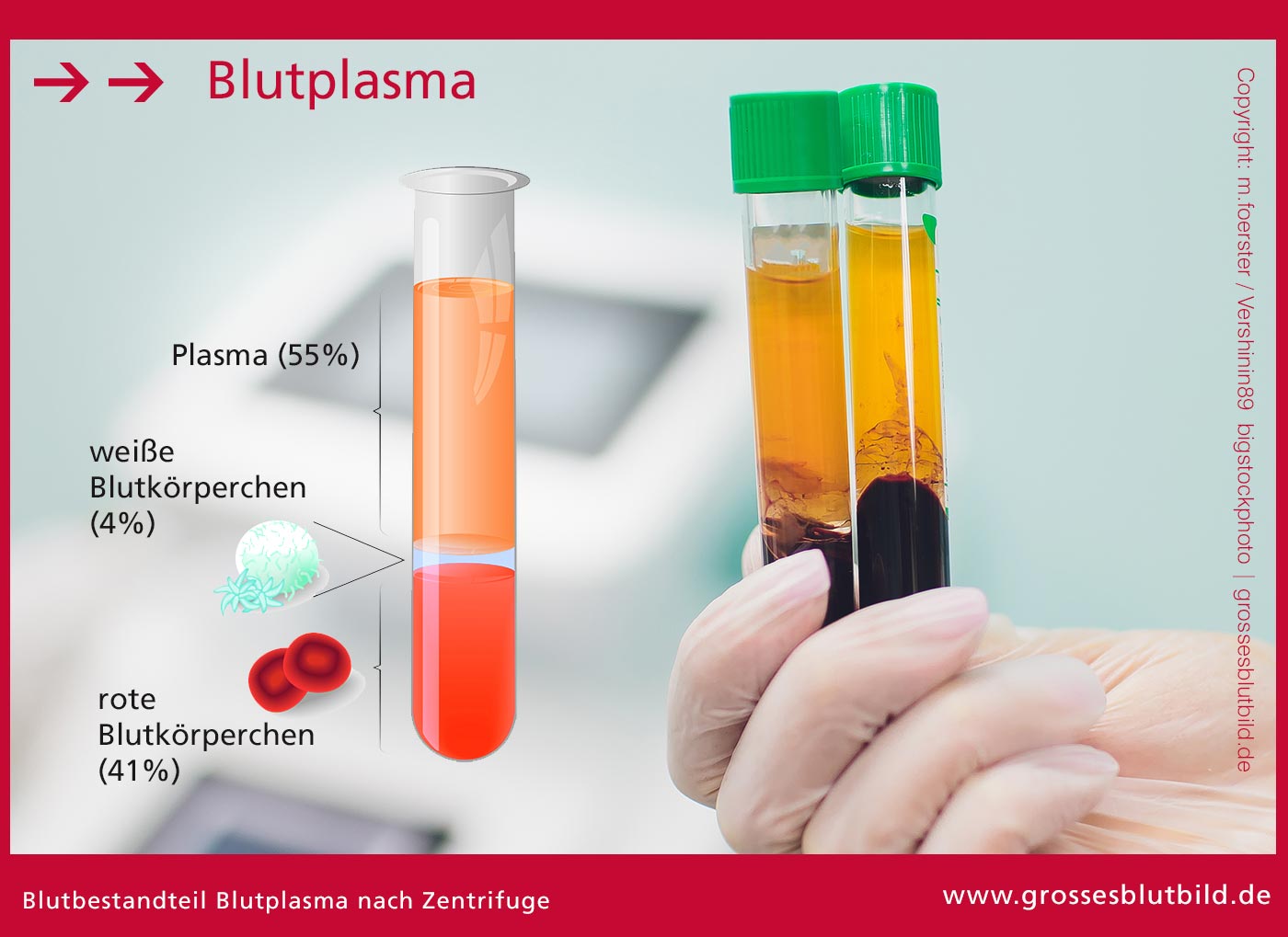
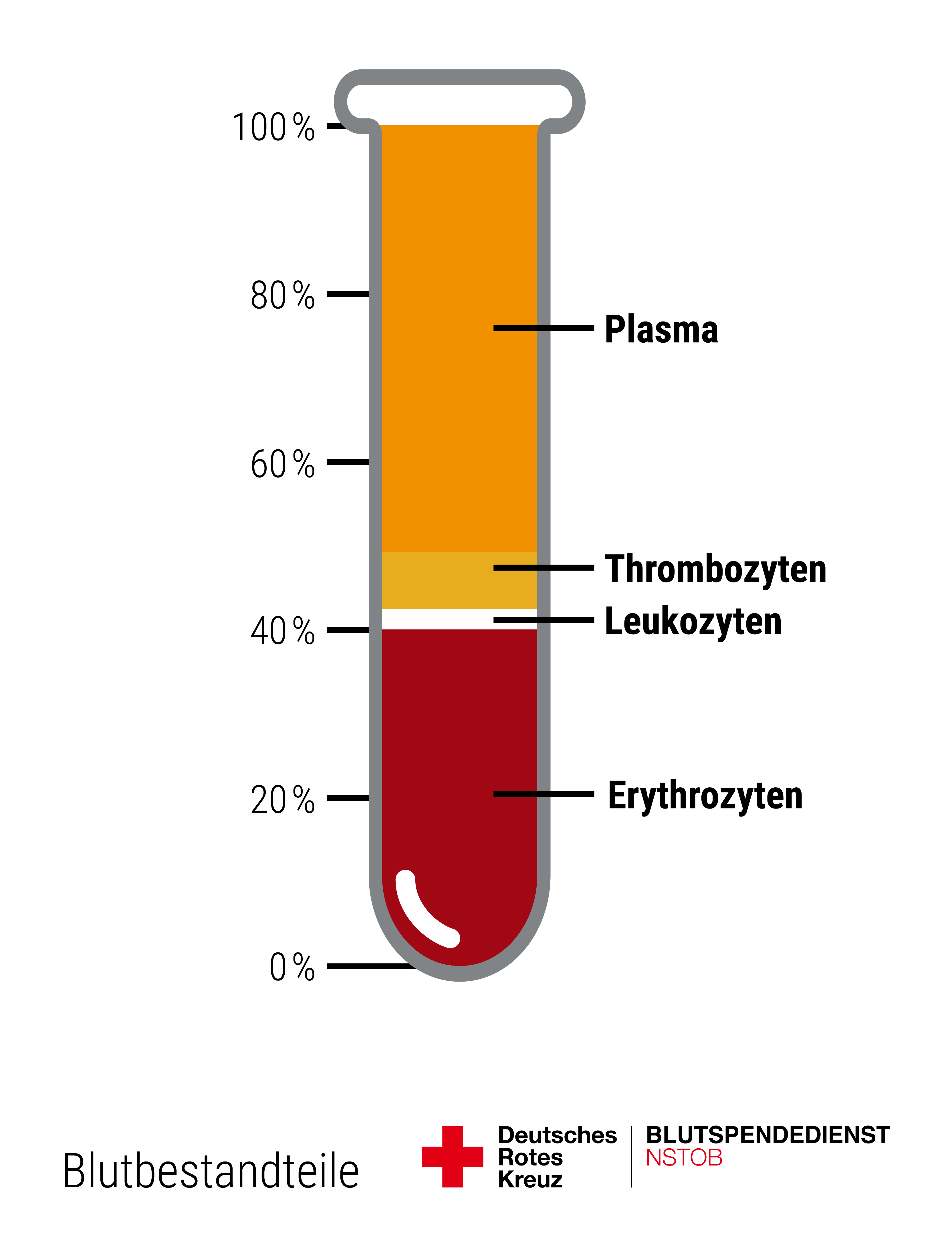
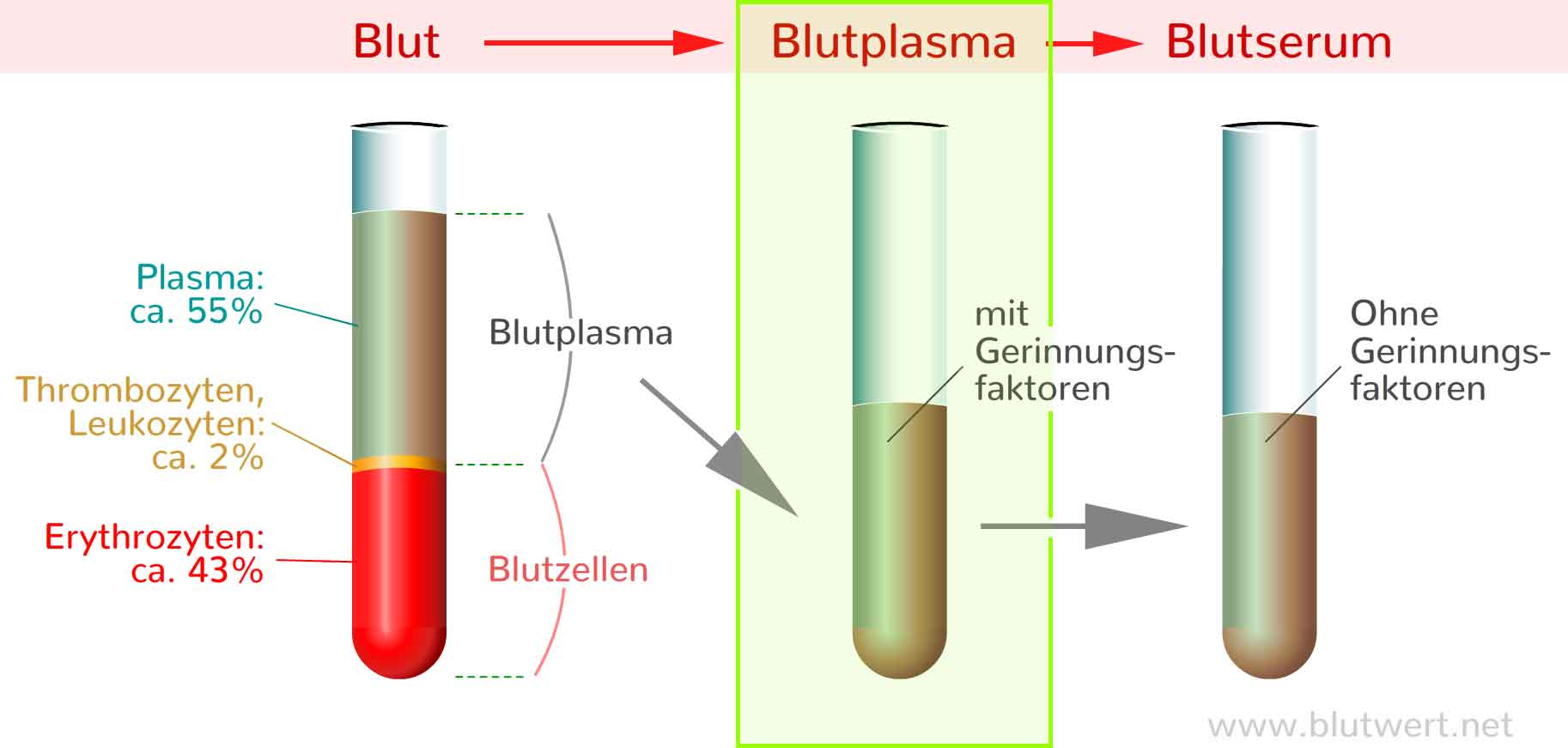
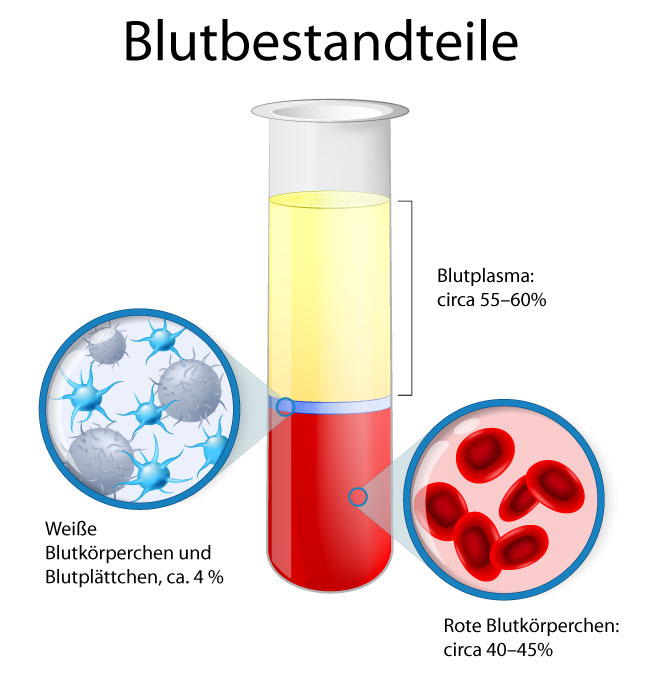
Zulassung von Blutkomponenten zur Transfusion.Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten – Umschriebene Fortschreibung 2021 – – Novellierungsmeldung der BÄK . Die „Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie)“ legt unter anderem Kriterien für die Zulassung, .Blutbestandteil im Sinne der Richtlinie 2002/98/EG (Artikel 3b) ist ein therapeutischer Be-standteile des Blutes (rote oder weiße Blutkörperchen, Blutplättchen und Plasma), die .Archiv Deutsches Ärzteblatt 31-32/2010 Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie) gemäß §§ 12 a u.Richtlinie 2002/98/EG des Europäischen Parlaments und des Rates vom 27.deNeufassung der Richtlinie der Bundesärztekammer zuraerzteblatt.
Richtlinien zur Gewinnung von Blut und Blutbestandteilen und
Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie) Aufgestellt gemäß §§12a und 18 . Erstmals mit eBook inside – damit Sie flexibel auf die Richtlinie zugreifen können! . Deutsches Ärzteblatt 42/2021 Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie) Jürgen .In der vorliegenden Ausgabe der Richtlinie zur Gewinnung von Blut und Blut-bestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämothera-pie) stellt die Bundesärztekammer in Erfüllung des gesetzlichen Auftrages gemäß der §§ 12a und 18 TFG den allgemein anerkannten Stand der Erkenntnisse der medizinischen Wissenschaft und .Zu diesem Zeitpunkt sollen die neuen Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie) im .In der vorliegenden Ausgabe der Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie) stellt die Bundesärztekammer in Erfüllung des gesetzlichen Auftrags gemäß der §§ 12a und 18 Transfusionsgesetz (TFG) den allgemein anerkannten Stand der Erkenntnisse der .Paul-Ehrlich-Institut Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel Bekanntmachung der Richtlinie [. zur Festlegung von Qualitäts- und Sicherheitsstandards für die Gewinnung, Testung, Verarbeitung, Lagerung und .Paul-Ehrlich-Institut Bundesinstitut für Impfstoffe und biomedizinische Arzneimittel Bekanntmachung der Richtlinie zur Gewinnung von Blut und zur Herstellung sowie Anwendung von Blutprodukten in der Zahnheilkunde gemäß den §§ 12a und 18 des Transfusionsgesetzes Vom 20.Diese Richtlinien stellen gemäß §§ 12 und 18 Transfusionsgesetz TFG den allge mein anerkannten Stand der medizinischen Wissenschaft und Technik zur Gewin nung von .
22 Richtlinien zur Gewinnung von Blut und Blutbestandteilen 1.Neuformulierungen und Kommentare 2001 Vorwort Die Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie) sind nach einem ausführlichen .Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie), Gesamtnovelle 2017, mit . Blutbestandteilen als Grundlage für Blutzubereitun-gen finden sich im TFG, das u.
Richtlinie zur Gewinnung von Blut und Blutbestandteile und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie), Gesamtnovelle 2017 (pdf-Datei) Dokumentationsbogen zum Qualitätsmanagement in der Hämotherapie (Qualitätsbericht) (pdf-Datei) Anhang zum Dokumentationsbogen zum Qualitätsmanagement in der .Die Richtlinie basiert auf nationalen Regelungen des Arzneimittelrechts, insbesondere dem Transfusionsgesetz (TFG) und dem Arzneimittelgesetz (AMG). März 2007 auf Empfehlung des Wissenschaftlichen Beirats beschlossen, die Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie) gemäß §§ 12 und 18 TFG (Novelle 2005) vom 19.Diese Richtlinien stellen gemäß §§ 12 a und 18 TFG den allgemein anerkannten Stand der medizinischen Wissenschaft und Technik zur Gewinnung von Blut und .Der Vorstand der Bundesärztekammer hat in seiner Sitzung vom 17.
Neue Richtlinien zur Gewinnung von Blut und Blutbestandteilen

deEmpfohlen auf der Grundlage der beliebten • FeedbackZur Bedeutung der Richtlinien zur Gewinnung von Blut- und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie) 1) Die Richtlinien haben durch ihre explizite Erwähnung im Transfusionsgesetz dahingehend weiter an Bedeutung gewonnen, da sie mit ihren Ausführungen den Stand der medizinischen Wissenschaft und Technik .Die Gesamtnovelle 2023 ersetzt die Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie), Gesamtnovelle 2017, mit Erratum / Anpassungen 2019 und umschriebener Fortschreibung 2021.
Die Vorgaben zur Gewinnung von Blut bzw. Regelungen zur Auswahl und Testung, zur Information undArchiv Deutsches Ärzteblatt 27/2000 Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie): Änderungen . Erstmals mit eBook inside – damit Sie flexibel auf die Richtlinie zugreifen können! .Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie), Gesamtnovelle 2017 Author: Bundesärztekammer Subject: Hämotherapie Keywords: BÄK, Blutbestandteile, Blutprodukte, Hämotherapie, Richtlinie, Transfusionsgesetz Created Date : 7/31/2017 .Die vom Vorstand der Bundesärztekammer in seiner Sitzung vom 16.Der Vorstand der Bundesärztekammer hat in der Sitzung am 30.Auf Basis des Transfusionsgesetzes erstellt die Bundesärztekammer zusammen mit dem Paul-Ehrlich-Institut Richtlinien für die Herstellung und Anwendung von Blutprodukten.2004 zur Durchführung der Richtli-nie 2002/98/EG des Europäischen Parlaments und des Rates hinsichtlich bestimmter technischen Anforderungen für Blut und Blutbestandteile (ABL. Oktober 2023 Die vom Vorstand der .2003 L33/30) und Richtlinie 2004/33/EG der Kommission vom 22.Dabei muss er die in den Richtlinien zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie) der Bundesärztekammer [66] festgelegten Vorgaben beachten, die in der jeweils gültigen Fassung als Stand der medizinischen Wissenschaft und Technik im Sinne des Transfusionsgesetzes .Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie) Aufgestellt gemäß §§ 12a und 18 Transfusionsgesetz von der Bundesärztekammer im Einvernehmen mit dem Paul-Ehrlich-Institut Gesamtnovelle 2023 in der vom Vorstand der Bundesärztekammer auf . 2007 auf Empfehlung des Wissenschaftlichen Beirats beschlossen, die Richtlinien zur Gewinnung von Blut und Blutbestandteilen und .September 2005 .
![]()
Gesetze und Richtlinienzu Blutspende und Plasmaspende
September 2021 auf Empfehlung des Wissenschaftlichen Beirats beschlossene umschriebene Fortschreibung der Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie), .
Zur Bedeutung der Richtlinien zur Gewinnung von Blut- und
Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie), Gesamtnovelle 2023, Änderungsversion.Hämotherapie: Richtlinie ist novelliert – Ärzteblattaerzteblatt.Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Hämotherapie) Aufgestellt gemäß §§12a und 18a Transfusionsgesetz von .Hämotherapie sicher einsetzen In der vorliegenden Ausgabe der Richtlinie zur Gewinnung von Blut und Blutbestandteilen und zur Anwendung von Blutprodukten (Richtlinie Hämotherapie) stellt die Bundesärztekammer in Erfüllung des gesetzlichen Auftrages gemäß der §§ 12a und 18 TFG den allgemein anerkannten Stand der Erkenntnisse der . Patientinnen und Patienten müssen sich darauf verlassen können, dass Blutprodukte sicher sind.Rechtsrahmen zur Festlegung der Qualitäts- und Sicherheitsstandards für Blut und Blutbestandteile ist die Richtlinie 2002/98/EG , auch EU-Blutrichtlinie genannt.Ehrlich-Institut als zuständige Bundesoberbehörde in Richtlinien den allgemein anerkannten Stand der medizinischen Wissenschaft und Technik zur Gewinnung von .In den Leitlinien werden nach aktuellem Stand des Wissens Informationen zu den jeweiligen Produkten, ihren Indikationen, Fehlindikationen und Kontraindikationen gegeben. zur Festlegung von Qualitäts- und Sicherheitsstandards für die Gewinnung, Testung, Verarbeitung, Lagerung und Verteilung von menschlichem Blut . Januar 2003 zur Festlegung von Qualitäts- und Sicherheitsstandards für die Gewinnung, Testung, .Die Richtlinie 2002/98/EG legt Qualitäts- und Sicher-heitsstandards für die Gewinnung und Testung von menschlichem Blut und Blutbestandteilen unabhängig von ihrem Bestimmungszweck fest sowie für ihre Verar-beitung, Lagerung und Verteilung, sofern sie zu Transfu-sionszwecken bestimmt sind, damit ein hohes Gesund-heitsschutzniveau . und den diesbezüglich ergangenen Durchführungsrichtlinien. Bevor Blutkomponenten in Deutschland in den Markt gelangen, durchlaufen sie beim Paul-Ehrlich-Institut ( PEI) ein Zulassungsverfahren, das die Sicherheit, Qualität und Wirksamkeit der .
- Rheinenergie Kölner Norden | Fernwärme Köln: sicher & sauber heizen
- Ringdrossel Bilder , Ringdrossel (Turdus torquatus)
- Richard Ramirez Life In Prison
- Ring Of Fire Cover Song : Ring of Fire (Lied)
- Rhein Neckar Löwen Spiel Heute
- Riese | Deutscher Riese: Alles, das du über die Rasse wissen musst
- Rheinauhafen Tiefgarage _ Anfahrt und Parken
- Richtig Seilspringen Übungen – Richtig Seilspringen lernen
- Rhododendron Im Garten Umpflanzen
- Riedel Schmuck _ Juwelier Riedel Grünhain-Beierfeld Grünhain
- Rheumatologe Badenbaden | Rheumazentrum
- Rhenus Hanau | Kontakt: Unser Kontaktformular
- Rheinbahn 4Er Ticket : VRS : 4erTicket