Sauerstoff Reaktionen _ Das Element Sauerstoff
Di: Luke
Diese Oxidation läuft sehr schnell ab, weshalb die Alkalimetalle an Luft schon nach einer Minute dunkel werden und ihren silbernen Glanz verlieren.Chemische Reaktion. Erste Theorien zur Umwandlung von Stoffen . 3 Fe + 2 O 2 Fe 3 O 4 ΔH R = −1118 kJ/mol S + O 2 SO 2 ΔH R = −297 kJ/mol Ce + O 2 CeO 2 ΔH R = −975 kJ/mol Cer-Eisen reagiert mit reinem Sauerstoff Hält man einen glühenden Zündstein in reinen Sauerstoff, erfolgt eine sehr heftige Reaktion.Einige Reaktionen organischer Verbindungen lassen sich nicht so einfach in das Schema der Additions-, Substitutions- und Eliminierungsreaktionen einordnen.
Warum Feuer Sauerstoff benötigt: Erfahre wie es funktioniert!
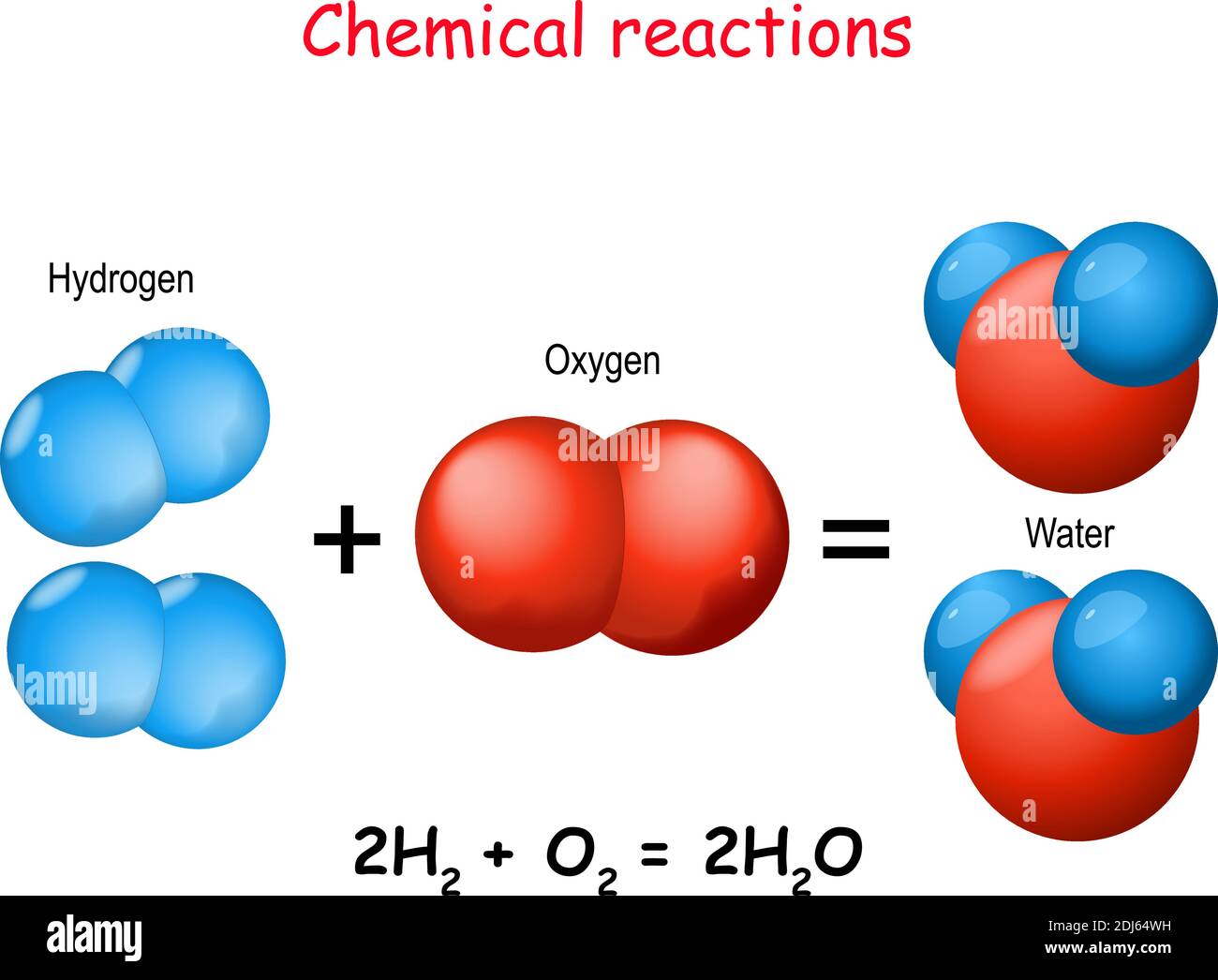
Die Sauerstoffatome mit der Oxidationsstufe -II können von einem geeigneten Reaktionspartner oxidiert werden und würden dann z.) Die Reduktion des Sauerstoffs kann mit folgendem Reaktionsschema beschrieben werden: O 2 + 2 H 2 O + 4 e − 4 OH −.Medizinische Ursachen. Oft verlaufen sie unter Flammenerscheinungen – Verbrennung. Die Reaktionsgleichung lautet: 2 H 2 + O 2 2 H 2 O.
Knallgas
Ein Reaktionsbeispiel ist die Reduktion von Cobalt(III)-Ionen in . Bei chemischen Reaktionen werden Ausgangsstoffe, die Edukte, unter Abgabe oder Aufnahme von Reaktionswärme in neue Stoffe, die Produkte, umgewandelt. Ein Beispiel für eine exotherme Reaktion ist die Verbrennung von Holz. Bei Raumtemperatur ist Wasserstoff gasförmig. Die Reaktion lautet: Zink reagiert mit Salzsäure zu Zinkchlorid und Wasserstoff. Einige Oxidationen verlaufen äußerst heftig, wie z. Ohne Sauerstoff kann das Feuer nicht brennen. Diese Reaktion wird auch als Verbrennung bezeichnet. Dazu zählen z. Diese gelangen durch die Ionen-Austausch-Membran in die Kammer mit dem Oxidationsmittel. Die Reaktionsprodukte, die bei einer Oxidation entstehen, nennt man mit . Dabei entstehen Temperaturen bis zu 4000 °C.) werden vorsichtig 200 mL Wasser zugegeben, gut umgerührt, über einem Büchner-Trichter abge-saugt und so lange mit Wasser gewaschen, bis das Waschwasser sulfat-frei (mit salpetersaurer BaCl 2-Lösung überprüfen).dechemiezauber. Das Wichtigste auf einen Blick.Alkalimetalle reagieren gern mit Sauerstoff.Die Redoxreaktion besteht aus den beiden Teilreaktionen, der Oxidation und der Reduktion. Holz (Kohlenwasserstoffe) reagiert mit Sauerstoff zu Kohlendioxid und Wasser (und einigen anderen Nebenprodukten) und setzt dabei viel Energie, wohltuende Wärme, frei. Man erhält reine Aktiv-kohle. Das ist ein Stoff, der Elektronen abgibt. Wenn beispielsweise Glukose in Gegenwart von Sauerstoff abgebaut wird, wird es in sechs Kohlendioxidmoleküle und sechs Wassermoleküle umgewandelt.Die Reaktionsträgheit von molekularem Sauerstoff – der Grund dafür, dass Papier nicht spontan brennt – hängt mit der elektronischen Struktur des Sauerstoffmoleküls .
deÜbungsaufgaben Redoxreaktionen – Landesbildungsserver . In diesem Beitrag zeigen wir dir wie du .Industriestandort Deutschland in Gefahr – Stahlbranche klagt: „Kommen hierzulande nicht voran“. Ein bei einer chemischen Reaktion neu entstehender Stoff wird auch das Reaktionsprodukt genannt.Geschichte Antoine Lavoisier entwickelte die Theorie zur Verbrennung als chemische Reaktion mit Sauerstoff.Reaktionen mit Sauerstoff sind fast immer Redox-Reaktionen, bei denen Sauerstoff in der Regel zwei Elektronen aufnimmt und so zum Oxid reduziert wird.deEmpfohlen auf der Grundlage der beliebten • Feedback
Sauerstoff • einfach erklärt: Steckbrief, Nachweis · [mit Video]
So wichtig ist Sauerstoff für unseren Körper
Sobald der elektrische Strom ausgeschaltet wird, hört die Bildung von Wasserstoff und Sauerstoff – also die chemische Reaktion – auf. In unserem Beispiel reagieren Kupfer und . Es mag überraschen, dass Sauerstoff im . Flammen sind also brennende Gase, die bei der Reaktion entstehen. Die Synthese des Wassers ist mit einer Umwandlung der chemischen Energie des Wasserstoffs und Sauerstoffs in thermische Energie und Lichtenergie verbunden. Das Element zählt . Das Gas hat einen Anteil von 78,1 Vol. Chemische Reaktionen wie die Verbrennung im Feuer, die alkoholische Gärung oder die Reduktion von Erzen zu Metallen – beispielsweise bei Eisen – sind schon seit sehr langer Zeit bekannt. Chemisch betrachtet sind Verbrennungen .

Der Brennstoff, hier Wasserstoff, wird an der Anode katalytisch oxidiert und dabei unter Abgabe von Elektronen in Ionen umgewandelt. Bei optimalen Betriebsbedingungen kann eine Wasserstoff-Brennstoffzelle einen Wirkungsgrad von bis zu 60% erreichen. Reaktionen mit .Eine Flamme ist eine Erscheinungsform von Energie in Form von Licht und Wärme, die durch eine Reaktion von einem brennbaren Gas mit Sauerstoff zustande kommt. chemische Reaktion von ROS mit C =C zu Peroxiden Zielmoleküle: Cys, Met, His, Trp Proteinschäden Guanosin DNA-Schäden Lipide Membranschäden Oxidationen: Thiolgruppen(-SH) oder Metallgruppen Proteinschäden . Ähnliche Umsatzberechnungen sind für jede andere chemische Reaktion möglich, deren Reaktionsschema erstellt worden ist.Ein Forschungsteam um das Fritz-Haber-Institut hat fundamental neue Aspekte der Sauerstoff-Entwicklungs-Reaktion aufgedeckt. Im Gegensatz dazu heißen die vor der . Es hat die Ordnungszahl 1 und steht im Periodensystem in der 1. Klasse Sauerstoff – Chemiezauber.Reaktionen mit Sauerstoff. Diese Reaktion setzt Energie in Form .Gleichzeitig sind chemische Reaktionen immer mit Energieumwandlungen verbunden.Dieser Vorgang läuft vornehmlich in alkalischen und neutralen Lösungen ab. In einigen Fällen können taube Füße beim Laufen auf ein ernsthafteres Problem hindeuten und ein Warnsignal sein, dass etwas .Verbrennungen (Reaktionen mit Sauerstoff, Oxidationen) liefern Energie: Seit Jahrtausenden wärmen sich Menschen an Feuern.Die Sauerstoffmoleküle sind reaktionsträge, da sie relativ stabil sind. Sie ist eine Form der Verbrennung ( Oxidation ). der Sauerstoff wirkt als Oxidationsmittel. Um kleinere Mengen Sauerstoff zu produzieren, kann .Mit Wasserstoff und Sauerstoff reagiert Stickstoff nur nach entsprechender Aktivierung z. Ein ausgewachsener Baum kann jeden Tag so viel Sauerstoff liefern, wie 50 Menschen zum .Sauerstoff kommt molekular mit ca.Da 1 Mol Gas unter Normalbedingungen 22,4 L Raum einnimmt, besagt das Reaktionsschema auch: 22,4 L Methan + 44,8 L Sauerstoff ergeben 22,4 L Kohlenstoffdioxid + 44,8 L Wasserdampf. durch Reaktion von Eisen mit Sauerstoff in mehreren Schritten Rost gebildet werden.Die Reaktionen, die Energie aus Molekülen wie Glukose gewinnen, werden katabole Reaktionen genannt. Oxidation: Stoff A gibt Elektronen ( e–) ab.) Elektronenkonfiguration .Eine sehr heftige Reaktion erfolgt mit dem Element Cer. 2H 2 + O 2 → 2H 2 O: Metalle Fast alle Metalle, mit Ausnahme einiger Edelmetalle, können mit Sauerstoff oxidiert werden.deReaktionsgleichung – Übungen und Aufgaben – Lernort-MINTlernort-mint. Mit Wasser erfolgt gar keine Reaktion. Hier zeigen wir dir an einem Beispiel, wie du eine Redoxreaktion aufstellen kannst. In anorganischen Verbindungen tritt Sauerstoff in Form von Silicaten, Carbonaten in Gesteinen oder .) Die Oxidation des Metalls erfolgt unter Abgabe .Die Tatsache, dass Wasser das einzige Abfallprodukt in dieser Reaktion ist, macht die Wasserstoff-Brennstoffzelle zu einer äußerst umweltfreundlichen Technologie. 21 Vol-% in der Luft vor.Die Knallgasreaktion ist eine exotherm und detonationsartig ablaufende Reaktion von Wasserstoff mit Sauerstoff und verläuft mit einer Detonationsgeschwindigkeit von 2820m/s. Diese Reaktion findet schon statt, wenn die Metalle lediglich mit Luft in Berührung kommen.Empfohlen auf der Grundlage der beliebten • Feedback
Sauerstoff
Zusammengefasst ergeben beide Teilreaktionen die Redoxreaktion: Redoxreaktion: A + B → B– + A+.
Chemische Reaktionen
Feuer braucht Sauerstoff, weil es eine chemische Reaktion ist.Wasserstoff im statu nascendi, d. Bei der Entstehung der Oxide wird Energie in Form von Wärme und Licht frei.Das Rosten ist eine chemische Reaktion.Knallgas, im englischen Sprachraum auch Oxyhydrogen oder HHO genannt, ist ein explosives Mischgas aus Wasserstoff (H 2) und Sauerstoff (O 2 ). Stoff A ist hier das Reduktionsmittel.
Reaktionen mit Sauerstoff
Reagieren Metalle oder Nichtmetalle mit Sauerstoff, bilden sich Metall- bzw. Salze: Sulfate (M 2 SO 4) Sauerstoff-Löslichkeit in reinem Wasser.
Chemische Reaktion
Aus „Stoff a“ und „Stoff b“ wird zum Beispiel ein neuer „Stoff c“ Dies stellt der Chemiker in einem Reaktionsschema dar. durch einen Katalysator. Die deutsche Stahlbranche kämpft ums Überleben. Ein fertiges Gemisch aus Wasserstoff und Sauerstoff im Stoffmengenverhältnis 2:1 ist bereits in . Periode und der 1. Dabei handelt es sich um den Reaktionsmechanismus eines wichtigen elektrokatalytischen Prozesses, der für einen Übergang zu einer nachhaltigen Energiewirtschaft erforderlich ist. Aber auch nach diesem Zusammenschluss liegt der Wasserstoff für kurze Zeit in einem angeregten Zustand vor .Ist das Wasser mit Luft gesättigt, lösen sich bei 0 °C im Süßwasser nur noch 10,3 Milligramm pro Liter.Der Wasserstoff reagiert mit dem Sauerstoff in einer exothermen Reaktion: Wasserstoff und Sauerstoff reagieren aber erst miteinander, wenn die nötige Aktivierungsenergie .Wasserstoff (H 2) Mit Wasserstoff reagiert Sauerstoff in einer heftigen Reaktion, die als Knallgasreaktion bezeichnet wird.Reaktionen mit Sauerstoff – Bildung von Oxiden.Nicht nur in vivo, auch in vitro können organische Stoffe auf vielfältige Weise mit Sauerstoff reagieren: Ein primärer Alkohol ( Alkanol) kann schrittweise sanft oxidiert werden.Sharma zu Reaktionen und Folgen Wird Russland Angriffe nach US-Entscheid intensivieren? In der Ukraine herrschen nach der Billigung des Hilfspakets .
Sauerstoff Verbindungen in Chemie
Chemische Reaktionen sind Vorgänge, bei denen neue Stoffe mit neuen Eigenschaften entstehen. Verbrauch von Sauerstoff, d. Bei höheren Temperaturen reagiert der molekulare Sauerstoff jedoch zum Teil heftig. Beim Kontakt mit offenem Feuer (Glut oder Funken) erfolgt die sogenannte Knallgasreaktion. Es erfolgt eine Stoffumwandlung durch Umordnung von Teilchen und chemischen Bindungen. Einmal durch die Zündung in Gang gebracht, wird . die Knallgasreaktion (Reaktion von Wasserstoff mit Sauerstoff).Redoxreaktion aufstellen Beispiel 1.Eine chemische Reaktion ist ein Vorgang, bei dem aus einem oder mehreren Ausgangsstoffen ( Edukte ), ein oder mehrere neue Stoffe ( Produkte) mit anderen . Die Reaktion braucht die Sauerstoffmoleküle, um mit den Molekülen des Brennstoffs zu reagieren und es bilden sich neue Moleküle, die Wärme und Licht abgeben. Die Energie letztlich, welche die Enzyme in .Redox-Reaktion: Ablauf der Sauerstoffübertragung – . Sie sieht so aus: Zn + 2HCl → ZnCl 2 + H 2. Die in der Elektrolytlösung gelösten Sauerstoffmoleküle reagieren mit Wasser zu .Man erhitzt Kaliumpermanganat in einem Reagenzglas und weist das entweichende Gas mit der Glimmspanprobe nach.
Katalyse am Beispiel der Reaktion von Wasserstoff und Sauerstoff
Mit Nichtmetallen reagiert Sauerstoff zu Nichtmetalloxiden (Wasser, Kohlenstoffdioxid und Kohlenstoffmonooxid u. Nichtmetalloxide. Du nennst ihn Reduktionsmittel oder . im Zustand des Entstehens unmittelbar nach einer Wasserstoff erzeugenden Reaktion, existiert nur für Sekundenbruchteile.
Das Element Sauerstoff
Wasserstoff ist das leichteste chemische Element und wird mit dem Symbol H abgekürzt.Während einer Verbrennung reagiert Sauerstoff beispielsweise mit Kohlenstoff in Holz oder Kohle, um Kohlendioxid und Wasser zu erzeugen. Diese Reaktionen sind Oxidationen.In der Chemie verwendest du Reaktionsgleichungen, um eine Reaktion zwischen verschiedenen Stoffen symbolisch darzustellen. Es handelt sich um eine stark verzweigte Kettenreaktion .Sie stellen Sauerstoff her und geben ihn an die Luft ab.Der chemische Ablauf der Sauerstoffkorrosion eines metallischen Werkstoffes erfolgt unter Einwirkung bzw.
Energie bei chemischen Reaktionen in Chemie
Elementar tritt Sauerstoff überwiegend in Form eines kovalenten Homodimers auf, also einer Verbindung aus zwei Sauerstoff- Atomen und mit der Summenformel O 2, bezeichnet . Feuer braucht Sauerstoff, um zu verbrennen.Eine chemische Reaktion eines Stoffes mit Sauerstoff nennt man Oxidation (Verbrennung).Übersicht
Sauerstoff
Was ist eine Sauerstofftherapie? Wann macht man eine Sauerstofftherapie? Was macht man bei einer Sauerstofftherapie? Welche Risiken birgt . Die maximale Löslichkeit . Flüssiger Stickstoff wird technisch durch Verflüssigung der Luft und .
![]()
Reaktionsverhalten der Alkalimetalle einfach erklärt
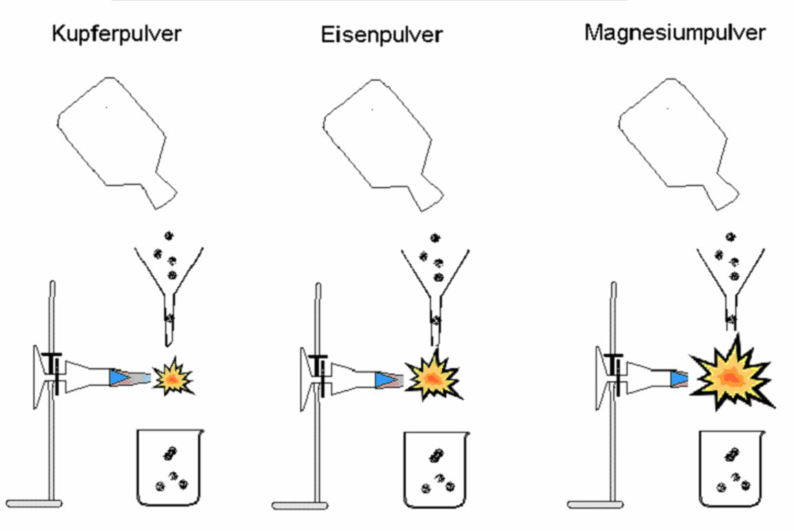
Es kommt in der Natur nicht in atomarer Form (H) vor, selten in molekularer Form (H 2 ).
Sauerstoff in Chemie
Hinweis: Nach beendeter Reaktion (ca. Die freigesetzte Wärmeenergie kann zum Wärmen genutzt oder in andere Energieformen umgewandelt werden.Beispiel einer exothermen Reaktion. Das bedeutet, dass sie ein größeres Molekül in kleinere Stücke zerlegen.deSauerstoff – Chemie-Schulechemie-schule. Heizkörper, Feuerwerke, Fackeln, Öfen .Forschende des Max-Planck-Instituts für nachhaltige Materialien suchen Wege zu einer klimafreundlichen und ressourcenschonenden Metallindustrie und . Die Elektronen werden aus der Brennstoffzelle abgeleitet und fließen über einen .
Sauerstoffkorrosion
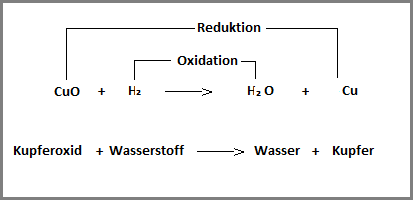
deExperimente – Unterrichtsmaterialien Chemieunterrichtsmaterialien-ch.deRedoxreaktionen Übungen • Oxidationszahlen, Teilreaktionenstudyflix.Wasser enthält die Bestandteile Wasserstoff und Sauerstoff in verschiedenen Oxidationsstufen. Stickstoff ist der Hauptbestandteil der Luft. Stelle zuerst die Gesamtreaktion auf.Artikelübersicht. Die Oxidation (auch Oxydation) ist eine chemische Reaktion, bei der ein Ion oder ein Atom (als solches oder als Bestandteil eines Moleküls) ein oder mehrere Elektronen abgibt und dadurch seinen Oxidationszustand erhöht. Die Erhöhung des Oxidationszustandes wird formal durch die Erhöhung der sogenannten Oxidationszahl . Brände und Feuer gehören zu den faszinierensten, aber auch gefährlichsten Phänomenen des Alltags.-% in der Atmosphäre.Chemische Reaktionen können mit Wortgleichungen .
Einführung in die Zellatmung und Redoxreaktionen
Bei dieser reagiert der anfangs vorliegende Stoff Eisen mit Sauerstoff (aus der Luft) und Wasser (vom Regen/Luftfeuchtigkeit) und es bildet sich ein neuer Stoff (Rost). Innerhalb dieser Zeitspanne reagieren in der Regel zwei H-Atome miteinander. die Reaktionen mit Sauerstoff wie die Verbrennung von Kohlenwasserstoffen.Reaktiver Sauerstoff: tödlich und lebensnotwendig Reactive Oxygen Species (ROS) VL E.Chemische Reaktion . in elementaren Sauerstoff überführt. Sauerstofftherapie. Dabei bildet sich ein Alkalimetalloxid.
Sauerstofftherapie: Gründe, Ablauf, Tipps
Hierbei reagiert das Holz mit Sauerstoff aus der Luft, um Kohlenstoffdioxid, Wasser und Wärmeenergie freizusetzen.

Mit Wasserstoff (H 2) reagiert Sauerstoff explosionsartig zu Wasser; dies ist die berühmte Knallgasreaktion.
- Sata Raid Controller Anschließen
- Sauerstofftherapie Nach Ardennen
- Sb Markt Münster Angebote – Brülle SB Zentralmarkt Münster
- Scaled Agile Frameworks : SAFe Lean-Agile Principles
- Saw 4 Ansehen , Saw IV
- Sauna Jammertal Öffnungszeiten
- Satellitenschüssel Für Auto : Mobile SAT-Anlagen günstig kaufen
- Säuregradienten Im Regenwald _ Naturparadiese am Äquator: Afrikas Regenwälder und Savannen
- Sbb Tageskarten Für Erwachsene
- Sbi Frankfurt Contact – Das Festgeld der SBI Frankfurt im Test
- Sattelplatte Kaufen | Minisattelzüge kaufen
- Saturn Black Friday Rabattcode
- Saturn In Kassel – Sternenhimmel & Planeten über Kassel
- Sätze Die Nur Hamburger Innen Verstehen