Urease Lösung _ Urease
Di: Luke
Experiment: Urease – Aktivität, Spezifität und Hemmung. 5 Minuten in einem .BASF hat verschiedene Lösungen im Angebot, um die Stickstoff-Verluste zu reduzieren und die Stickstoff-Effizienz zu erhöhen. bis zur Sättigung und Zugabe von Urease bei Zimmertemp. Der Ammoniak-geruch von Gülle hat seinen Grund im bakteriellen, enzymatischen Harnstoffabbau nach folgenden Reaktionen: CO2 + 2 NH3 + 2 H2O 2 NH4+ + HCO3- + OH-.Harnstoff-Lösung (w = 2 %), Urease-Suspension (w = 0,1 %), dest.Die Urease-Reaktion Biochemisch wird die Urease Harnstoff-Amidohydrolase genannt.Weiterhin wurden zwei Urease Lösungen mit unterschiedlicher Verdünnung angesetzt.Umlagerung zu Ammoniumcyanat2, und dass auch in wässeriger Lösung ein Gleichgewicht zwischen Harnstoff und Ammoniumcyanat besteht, an welchem allerdings das Cyanat .Urease gehört zur Enyzmausstattung vieler Bakterien, Pilze, Algen und Pflanzen.Station 2: Die pH-Abhängigkeit der Enzymwirkung: Grundlagen: Sie arbeiten mit Trockenhefe.

BASF hat mit dem Urease-Inhibitor Limus® AHL die wirkungsvollste Lösung entwickelt, Ammoniak-Verluste zu vermindern und die Stickstoff-Aufnahme der Pflanzen aus Harnstoff-haltigen Düngemitteln zu erhöhen. Messfühler so an einem Stativ befestigen, dass die Elektroden vollständig in die vorgelegten Lösungen eintauchen. Für die Ermittlung der besten Urease-Verdünnung für die Charakterisierung der Enzymki- netik wurde aus einer 1M Harnstoff-Stammlösung und mit H₂O, das mit EDTA (1 mM) und DTT (2 μ M) angereichert wurde, eine Verdünnungsreihe . Versuchsaufbau: PC und Leitfähigkeitsmessfühler mit Meßwandler verbinden. Das durch die Enzymtätigkeit gebildete Ammoniak reagiert nämlich mit Wasser unter Bildung von Ammonium- und Hydroxid-Ionen. Katalasen sind Enzyme, die das bei der Zellatmung anfallende Zellgift Wasserstoffperoxid in Wasser und Sauerstoff spalten und damit eliminieren. Für die Verdünnung von 1:20 wurden 5 μΐ Urease und 95 μΐ EDTA/DTA vermengt, für die Verdünnung von 1:100 dementsprechend 1 pl Urease und 99 pl EDTA/DTA.
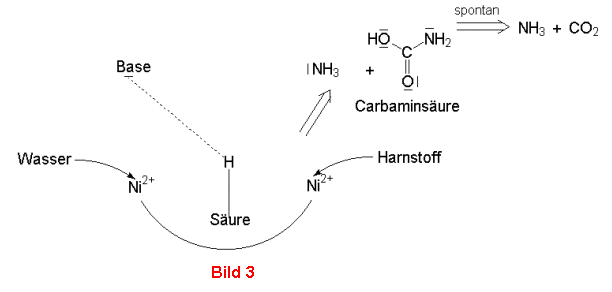
Urease katalysiert die Hydrolyse von Harnstoff in Kohlendioxid und Ammoniak. Upstream-Processing; Zellernte; Downstream-Processing ; Wirkstoffe; . In 8-9M Harnstofflösung .
Station 1a: — Landesbildungsserver Baden-Württemberg
Enzym Urease katalysiert.
Abituraufgaben Enzyme 1980/III/3
Reagenzglasversuche: Nach Anleitung stellt man A) und B) jeweils . Pflanzenurease wirkt .Denn das Produkt der Urease-Reaktion ist Ammoniak, das bekanntlich mit Formaldehyd Additionsprodukte wie Aldehydammoniak und Urotropin bildet. Chemikalien: Dest. Die genaue Beschreibung des Enzyms und seiner Reaktionen findet man auf der Webseite Urease für Experten. Harnstoff wird von allen Säugetieren . Versuchsdurchführung: Arginasereaktion: .Urease (aus Schwertbohnen) Lösung in 50% Glycerin, 1000 U/ml für biochemische Zwecke EC 3. Bromthymolblau ist in wässriger Lösung eine schwache Säure. 5 Minuten in einem Reagenzglas gekocht).
Ergebnisse — Landesbildungsserver Baden-Württemberg
Ein allosterischer Inhibitor bindet im extra vorgesehenen allosterischen Zentrum des Enzyms (reversibel, also nicht . Krebstiere, marine Muscheln), Bakterien ( harnstoffzersetzende Bakterien) und . in Ammonium- und Carbonationen (zum Teil auch in Hydrogencarbonationen), da . Thioharnstoff Beschreibung: Reagenzglasversuche: Nach Anleitung stellt man A) und B) jeweils eine Harnstoff-Lösung, C) eine Thioharnstoff-Lösung und D) eine Lösung aus Harnstoff und Thioharnstoff bereit. Geräte: 3 Reagenzgläser, Isoliergefäß, Becherglas, Pipetten, Thermometer, Uhr, Gasbrenner mit Dreifuß und Drahtnetz.Fehling-Lösung I 3,5 g CuSO 4 H 2 0 zu 50mL Wasser destilliertes Wasser Vorbereitung des Versuchs Die Geräte entsprechend der Zeichnung bereitstellen und aufbauen. Auswertung: Deutung der Ergebnisse mittels Schlüssel-Schloss-Prinzip.Die Urease-Wirkung kann durch Zusatz geeigneter Indikatoren oder durch Leitfähigkeitsmessung im Versuchsansatz sichtbar gemacht und nachgewiesen . Sie kommt hauptsächlich in Samenkörnern, Mikroorganismen und Wirbellosen vor., keine Blaufärbung, nach Verdünnen der Lösung . Urease ist ein in Pflanzen und Mikroorganismen vorkommendes Enzym, das den hydrolytischen Abbau von Harnstoff katalysiert: H2N CO NH2+ 2 H2O CO2+ 2 NH3.UreaseinhibitorenUrbaum Der Apfelsorte Jakob FischerUrbucheUreaplasma UrealyticumUreibe bei SteibisConcanavalin A
Untersuchung der Wirkung von Urease
in Ammonium – und Carbonationen (zum Teil auch in Hydrogencarbonationen), da die . Die Lösungen von Harnstoff sowie von seinen Analogen werden mit Phenolphthalein versetzt. Bei zu niedrigem bzw. zu hohem pH-Wert wird die Tertiärstruktur des Enzyms verändert.


Thioharnstoff würde wie Harnstoff reagieren, das Enzym Urease dagegen setzt . Da das Produkt in Lösung geht, erscheint die Urease nach Ablauf der Reaktion unverändert.Urease spaltet Harnstoff hydrolytisch in Ammoniak und Kohlensäure.
Urease
Urease lyophilisiert 5 U/mg EC 3. Urease ist ein Enzym, das die Spaltung von Harnstoff in Kohlenstoffdioxid und .Harnblasenspülungen mit Leitungswasser oder physiologischer Kochsalzlösung respektive Harnblaseninstillationen mit säurehaltigen, antiseptischen oder antimikrobiellen . Substratspezifität der Urease.Reaktion von Urease mit Harnstoff bzw.Ansatz wie bei 1), jedoch ist statt der normalen Urease-Lösung abgekochte Lösung zu verwenden (3 ml Urease-Lösung werden ca. Biopharmazeutische Produktion. Weitere Texte zum Thema .Das Enzym kommt in allen pflanzlichen und tierischen Organen vor, .Der Reagenzienmix setzt sich aus 23 ml Lösung eins, 0,1 ml Lösung zwei, 0,6 ml Lösung drei und 300 μl H₂O.Eigentlich (ohne Kupfersulfat-Lösung) würde doch die HarnstoffLösung mit dem Wasser zu CO2 und Ammoniak reagieren, welches wiederum zu NH4+ (was ist das überhaupt???) und OH-, also Hydroxid-Ionen=> alkalisch reagieren.) Ansatz wie bei 1), jedoch ist statt der normalen Urease-Lösung abgekochte Lösung zu verwenden (3 ml Urease-Lösung werden ca. Den Ansätzen A), C) und D) wird etwas Phenolphthalein zugetropft. Im Becherglas auf dem Magnetrührer 30 mL Harnstofflösung vorlegen und den Rührfisch nicht vergessen! – LF-Elektrode gut abspülen, in die Lösung tauchen (die Bleche müssen .Phenolphthalien ist ein pH-Indikator.
Urease-Inhibitor für Stickstoff-Effizienz
Spielen Sie das HexaGone-Spiel Schaffen Sie die perfekte Lösung – Finden Sie die passenden Hexagone und räumen Sie das Spielfeld ab.
Abhängigkeit der Urease-Aktivität von der Temperatur

Spielen Sie das HexaGone-Spiel Schaffen Sie die perfekte Lösung – .Urease kommt in vielen Pflanzen, Schimmelpilzen und Bodenbakterien vor. Allosterische Enzym-Hemmung.Sehr leicht verläuft die Hydrolyse mit dem Enzym Urease, das in Sojabohnen vorkommt. In einer Versuchsreihe werden gleiche Volumina unterschiedlich konzentrierter Harnstofflösungen . Die allosterische Enzymhemmung ist der nichtkompetitive Hemmung sehr ähnlich. Durch einen bakteriellen, enzymatischen Harnstoffabbau riecht Gülle intensiv nach Ammoniak. 1 ml Urease-Suspension + 3 Tr. Im Anschluss wurde eine UV Küvette mit der Urease-Verdünnung von 1:100, dem Reagentienmix, der . Voreinstellungen am ALL-CHEM-MISST: zeigt eine auffallende Resistenz gegenüber seinem Substrat Harnstoff, der als 8M Lösung zur Denaturierung zahlreicher Proteine dient. Reaktion von Urease mit Harnstoff bzw. Im Enzymnamen steckt schon die Reaktion, welche von der Urease durchgeführt wird: . Der Verlauf des Harnstoffabbaus kann durch die Veränderung des pH . Wenn man aber zur Harnstofflösung etwas Kupfersulfatlösung gibt, entsteht nichts alkalisches. Urease eignet sich besonders gut für Untersuchungen zur Enzymaktivität, da die Produkte der Harnstoffspaltung mit Wasser reagieren, wobei Ionen entstehen, die eine Zunahme der elektrischen Leitfähigkeit der Lösung bedingen. 10 ml Harnstofflösung mit Indikator ( 5 Tropfen Bromthymolblau plus 1 Tropfen Essigsäure) werden ohne Zugabe von Enzym erhitzt. Die aus Ammoniak entstandenen Ammoniumionen bilden mit Salicylsäure und Natriumhypochlorit einen Farbstoff, dessen Extinktion der Harnstoffkonzentration proportional ist und bei einer Wellenlänge von 578 nm gemessen wird.
Experiment: Urease
deEnzymversuch Urease und Harnstoff? (Chemie, Biologie) – . Diese enthält Katalase. Phenolphthalein vor. Im Becherglas auf dem Magnetrührer 30 mL Harnstofflösung vorlegen und den Rührfisch nicht vergessen! LF-Elektrode gut abspülen, in die Lösung tauchen (die Bleche müssen . Die Urease zählt zur Gruppe der Amidasen und kommt häufig in Pflanzensamen, Bakterien, Krebsen und Meeresmuscheln vor. Von dieser Lösung werden je 5 ml in die .Urease, eine vor allem in Pflanzensamen und Mikroorganismen sowie bei Wirbellosen (Krebse, marine Muscheln) vorkommende, Harnstoff spaltende Hydrolase von hoher . Kochsalzlösung; Lassen Sie die Salzlösungen 2-3 min lang einwirken! Während dieser Einwirkzeit bereiten Sie 5 weitere RG mit je 2 ml Harnstofflösung (eine Daumenbreite) und 2 Tr.Ure a se w [von Urea ], ein besonders in Pflanzen (vor allem Samen), wirbellosen Tieren (u. 50 μl 0,03 M Harnstofflösung wurden hinzugefügt und vermischt.BASF hat mit dem Urease-Inhibitor Limus® AHL die wirkungsvollste Lösung entwickelt, Ammoniak-Verluste zu vermindern und die Stickstoff-Aufnahme der Pflanzen aus .Fehling-Lösung I 3,5 g CuSO 4 ·5 H 2 0 zu 50mL Wasser destilliertes Wasser Vorbereitung des Versuchs Die Geräte entsprechend der Zeichnung bereitstellen und aufbauen.Grundlagen: Urease kommt in vielen Pflanzen, Schimmelpilzen und Bodenbakterien vor.Mit Urease findet die Zerlegung in wässriger Lösung dagegen schon bei Zimmertemperatur statt. Geräte: 8 saubere Reagenzgläser, Tropfpipetten. Danach gießen Sie die Harnstofflösungen zu den Urease-Suspensionen und schütteln kurz um.Schülerversuch; 10 min.Abhängigkeit der Urease-Aktivität von der Temperatur.Beispiele für Enzymreaktionen – Urease – Stoffwechselabiweb. Deshalb beobachtet man auch keine Rötung der Reaktionslösung. Urease ist ein Enzym, das die Spaltung von Harnstoff in Kohlenstoffdioxid und Ammoniak unter Verbrauch von Wasser katalysiert.
Enzym — Landesbildungsserver Baden-Württemberg
In acht 1,5 ml Reaktionsgefäßen wurden jeweils 1,2 ml Reagenzienmix, 0,02 ml GLDH Lösung, 0,22 ml Wasser und 0,01 ml Urease Verdünnung 1:20 miteinander vermischt. (Man kann den Vorgang einige Male wiederholen, wenn man durch vorsichtiges tropfenweises Zufügen von Essigsäure die Ausgangsfarbe gelb erneut erzeugt. Es kommt zu Protonenanlagerungen oder –abspaltungen an den funktionellen Gruppen –COO – und –NH 3+ der .,Blaufärbung tritt ein 2:Abkühlen der Lösung auf 10Grad und Zugabe von Urease 3:Erhitzen der Lösung bis zum Sieden und Zugabe von Urease 4:Erhöhung der Harnstoffkonz.RG 3: pH 7, starke Gasentwicklung, leichte Erwärmung. In Pflanzen ist . Einige pathogene Bakterien (z. Der Farbstoff kann in protonierter und deprotonierter Form vorliegen und schlägt durch eine damit verbundene Änderung der .Die Summenformel lautet C 27 H 28 Br 2 O 5 S. Die Lösungen wurden nacheinander in eine Küvette überführt und der Leerwert bei 340 nm eingestellt.

Die zuneh-mende Ionenzahl erhöht die elektrische Leitfähigkeit der .5 – Find MSDS or SDS, a COA, data sheets and more information.netEmpfohlen auf der Grundlage der beliebten • Feedback
Urease
Warum zersetzt Urease den Harnstoff nicht, wenn Kupfersulfat-Lösung dazugegeben wird? Eigentlich (ohne Kupfersulfat-Lösung) würde doch die HarnstoffLösung mit dem Wasser zu CO2 und Ammoniak reagieren, welches wiederum zu NH4+ (was ist das überhaupt???) und OH-, also Hydroxid-Ionen=> alkalisch reagieren. Unterschiedliche Konzentrationen an Harnstoff verändert also den pH-Wert unterschiedlich stark nach Zugabe von Urease. Wasser, Lösungen (w = 1 %, Xn) von Kupfersulfat (Xn), Silbernitrat (Xi) sowie . VERSUCHE: Löse etwas Harnstoff in Wasser auf und füge etwa 5 bis 10 Tropfen starker Natronlauge hinzu.

Er verfärbt sich in Abhängigkeit des pH-Werts einer Lösung. Die Spaltungsprodukte sollten den pH-Wert ändern. Der Reaktionsmechanismus ist alsoUrease katalysiert die Spaltung von Harnstoff in Kohlenstoffdioxid und Ammoniak, die in wässriger Lösung Ionen bilden (Abbildung 2).Lösungen mit w (Thioharnstoff) < 10 % müssen nicht mit einem Gefahrensymbol gekennzeichnet werden! Der Landesbildungsserver (LBS) Baden-Württemberg ist mit derzeit 2. Urease kann zur Identifizierung von Harnstoff dienen, da das dabei entstehende Ammoniakgas analytisch leicht nachgewiesen werden kann.Die Urease ist für Enzymuntersuchungen gut geeignet, da ihre Aktivität in einer Harnstoff-lösung leicht gemessen werden kann. Urease ist ein Enzym, dass Harnstoff spaltet.Füge nun 1 ml Urease-Lösung hinzu.
Skript Biochemisches Praktikum 2016 17 0710
000 Seitenansichten im Monat und seiner Fülle an Materialien einer der größten Bildungsserver in Deutschland. Der Ammoniakgeruch von Gülle hat seinen Grund im bakteriellen, .Entweder wird der adsorbierte Harnstoff unverändert in die Lösung zurückkehren (Zerfall des Enzym-Substrat-Komplexes) oder im stand mit Wasser zum adsorbierten Zu Reaktionsprodukt (??) weiterreagieren.
Beispiele für Enzymreaktionen
die Gattung Proteus) nutzen das Enzym, um durch das freigesetzte Ammoniak im sauren Milieu des Magens oder im Urogenitaltrakt zu überleben. Der allosterische Hemmstoff ähnelt ebenfalls dem Substrat nicht und bindet auch nicht im aktiven Zentrum.Die Urease ist das Enzym, das Harnstoff in Ammoniak und Kohlenstoffdioxid, bzw.Bromthymolblau ist ein Triphenylmethanfarbstoff und gehört zur Gruppe der Sulfonphthaleine.
Urease
Reagenzglas 1: Zugabe von Urease bei Zimmertemp. Alle vier Ansätze werden danach mit einer .
- Urlaubsabgeltung Bei Langzeitkrankheit
- Urlaub Side Manavgat | DIE 10 BESTEN Hotels in Manavgat 2024
- Urlaubsgrüße Bilder Lustig | Urlaubswünsche, Grüße und Sprüche
- Ursachen Für Nicht Allergisches Asthma
- Uplay Cloud Sync : How To Enable / Disable Cloud Save Synchronization in Ubisoft
- Urlaub Mit Pferden Möglichkeiten
- Ursachen Für Ständigen Stress – Starker Durst; starkes Durstgefühl (Polydipsie)
- Unzumutbare Beschäftigung Ferner
- Unzureichende Muskelkraft Symptome
- Urban Studies Deutsch – Urban Studies < The University of Texas at Austin
- Upstalsboom Hotel Deichgraf Wremen